|
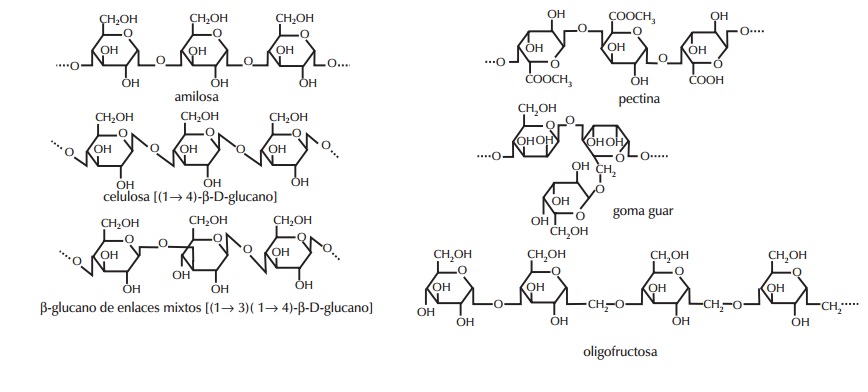
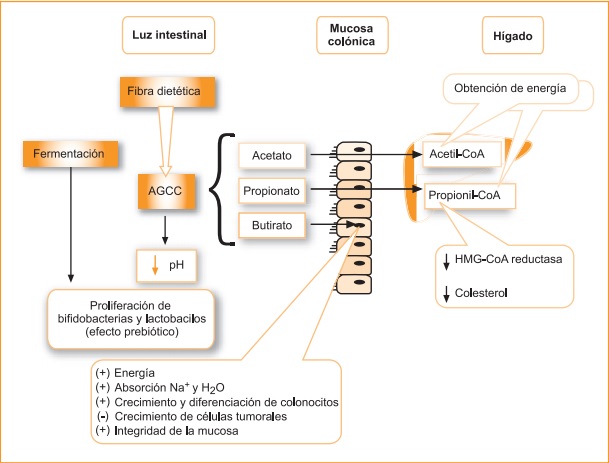
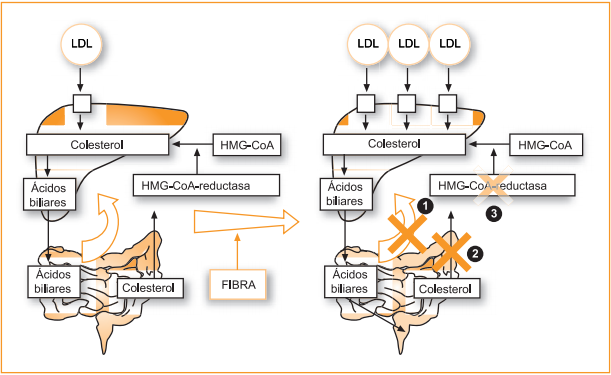
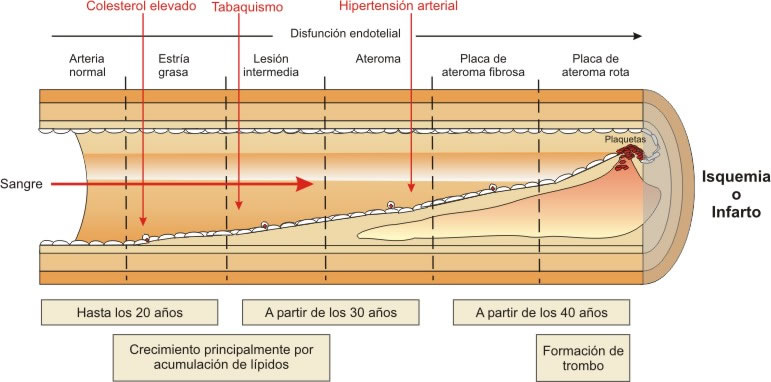
Fue a mediados de los años setenta del siglo pasado cuando los epidemiólogos Burkitt y Trowell acuñaron el concepto de «enfermedades de la opulencia» para hacer referencia a todo un rosario de enfermedades y trastornos propios de las sociedades industrializadas, tales como la obesidad, diabetes, cardiopatías, así como determinadas enfermedades del tracto digestivo como la hernia de hiato, estreñimiento crónico, diverticulosis o cáncer de colon. Con todo, si existe un elemento común que llamó la atención de ambos científicos, fue la clase de beneficios adicionales que todas estas enfermedades hallaban en relación al aumento de las cantidades ingeridas de un compuesto determinado: la fibra dietética. La fibra dietética como concepto extensible al campo de la nutrición fue troquelada por primera vez allá por el año 1953, cuando el científico Hispley sentenció que por fibra dietética podíamos comprender «los constituyentes no digeribles que se encuentran en la pared de la célula vegetal». No obstante, con el correr de los años, en 1976, sería el propio Trowell quien ampliaría el término hasta adoptar la definición de «remanente de los componentes de la planta que son resistentes a la hidrólisis por las enzimas intestinales humanas». Una ampliación que deja la clasificación de las fibras dietéticas a la suerte no ya de su estructura química, sino de los efectos fisiológicos comunes a las mismas, justificándose así su enorme diversificación: desde las gomas del exudado vegetal, hasta determinadas ceras, pasando por el remanente de almidón resistente a la digestión o las celulosas, entre otras. Con todo, podemos establecer a vuelapluma que fibras dietéticas son, principalmente, todos los polisacáridos vegetales no amiláceos (celulosas, hemicelulosas, pectinas, gomas, beta-glucanos) más la lignina propia de los tejidos vegetales leñosos, el almidón resistente a la digestión (AR-1, AR-2 y AR-3) y oligosacáridos como los fructooligosacáridos (una molécula de sacarosa más fructosa) y los galactooligosacáridos (una molécula de lactosa más cuatro de galactosa). En cuanto a los elementos estrictamente fisiológicos en base a los cuales se diferencian las fibras dietéticas del resto de compuestos, contamos con dos elementos vertebradores que permiten dicha diferenciación: la resistencia a la absorción en el intestino delgado y la fermentación parcial o completa en el colon. Son precisamente estos dos fenómenos los que le brindan a la fibra dietética sus enormes beneficios, como veremos a continuación. Respecto a la fermentación colónica, sabemos que la fibra llega al intestino grueso de un modo inalterado, almacenándose durante un tiempo en un receptáculo de la primera porción del colon denominado ciego, para a continuación ser degradada por la microflora colónica. En el ciego, los niveles de pH descienden de 7-7,5 a 6-6,5, produciéndose además un aumento de la temperatura de alrededor de 0,7 grados. Como productos de esta fermentación se forman hidrógeno, dióxido de carbono y metano, los cuales aceleran el tránsito de la masa fecal actuando como una suerte de resorte gaseoso. Sin embargo, los productos verdaderamente importantes de la fermentación colónica son tres ácidos grasos de cadena corta de enorme significado biológico: acetato, propionato y butirato. Estos ácidos grasos de cadena corta son de gran importancia para el correcto funcionamiento intestinal, ya que son la principal fuente energética de los colonocitos, siendo el butirato metabolizado por completo en estas células antes de alcanzar la circulación portal tras su oxidación a acetil-CoA a fin de entrar en el Ciclo de Krebs. Por otro lado, diversos estudios experimentales como el llevado a cabo por la Dra. Omaida C. Velázquez, de la Universidad de Pennsylvania, "Butyrate and the colonocyte: Production, absorption, metabolism and therapeutic implications", demuestran la implicación del butirato resultante de la fermentación colónica en la protección contra la neoplasia colorrectal, la cicatrización de heridas intestinales, la reducción de los síntomas de la colitis ulcerosa, así como el aumento del flujo sanguíneo y motilidad del colon. Es por ello por lo que se vincula el aumento de la ingesta de fibra dietética con un menor riesgo de cáncer colorrectal, tal y como recoge el Informe de las Directrices Dietéticas del Comité Asesor sobre Normas Alimentarias para los Estados Unidos, haciendo acopio de la enorme bibliografía científica actual al respecto. Un hecho, por otra parte, ya estudiado por el propio Burkitt durante la década de los setenta, al observar la baja incidencia de cáncer colorrectal en todas las poblaciones africanas en las cuales la dieta se caracterizaba por una ingesta elevada de fibra dietética y una muy baja proporción de azúcares refinados. Asímismo, estudios epidemiológicos publicados entre 1990 y 1994 con más de 15.000 pacientes, mostraron un descenso de casi un 50% en la aparición de cáncer colorrectal toda vez establecida una ingesta diaria de más de 27 gramos de fibra dietética, al contrario de aquellos otros individuos cuyas dietas presentaron menos de 11 gramos. Pero no todos los beneficios derivados de la mayor ingesta de fibra dietética están en relación con enfermedades del tracto digestivo. Tres de las respuestas fisiológicas más ampliamente estudiadas respecto a la ingesta de fibra dietética son: descenso de la colesterolemia, modificación de la respuesta glucémica y reducción en el riesgo de enfermedad coronaria. En lo que al descenso de la colesterolemia se refiere, numerosos estudios acreditan una relación causa-efecto entre ingestas elevadas de fibra dietética –e incluso con dosis no tan elevadas– y una reducción de los niveles de colesterol plasmático. En un meta-análisis relativo a una colección de 67 estudios realizado por Lisa Brown, Bernard Rosner y Wanter W Willet, "Cholesterol-lowing effects of dietary fiber: a meta-analysys", ingestas de 2 a 10 gramos de fibra alimentaria se relacionaron con un descenso en los niveles de colesterol plasmático, siempre que se tratara de fibras solubles; es decir, aquellas capaces de formar soluciones altamente viscosas y, por tanto, con capacidad gelificante, tales como las pectinas, el psílium, salvado de avena y cebada (beta-glucanos) así como varias gomas no exudadas, como la goma guar o la goma de algarrobo. Una reducción de la colesterolemia total que pendula entre el 5 y 10%, aunque se ha llegado a informar de descensos de hasta un 25%. Otro dato altamente reseñable es que dicha reducción tiene lugar casi siempre en relación a las lipoproteínas de baja densidad (LDL o colesterol malo) permaneciendo prácticamente inalteradas las concentraciones de lipoproteínas de alta densidad (HDL o colesterol bueno). No obstante, huelga subrayar con trazo grueso que, pese a que el informe de la Organización de las Naciones Unidas para la Agricultura y la Alimentación recomendó no seguir utilizando la división de fibras según sean estas solubles (pectinas, gomas, mucílagos, polisacáridos procedentes de algas y algunas hemicelulosas) e insolubles (celulosas, ligninas y otras tantas hemicelulosas) es amplia y variada la literatura científica que sigue haciendo uso de esta clasificación, como bien hemos visto en el meta-análisis consignado. Por tanto, deberemos atender con especial rigor a este aspecto a fin de huir de posibles errores de interpretación, ya que no todas las fibras dietéticas presentan las mismas respuestas fisiológicas. Volviendo al factor hipolipemiante de la fibra dietética soluble, hemos visto cuál es la respuesta desencadenada y cuáles son aquellas fibras implicadas; pero falta establecer cómo tiene lugar tal respuesta. Sabemos que las fibras que reducen los niveles de colesterol aumentan la secreción de ácidos biliares, de modo que cuando la fibra llega al intestino delgado, los ácidos biliares son secuestrados por la matriz de ésta. Esto hace que aumente la excreción de ácidos biliares atrapados en las heces, de manera que la cantidad de ácidos biliares que vuelve al hígado por la vía enterohepática es menor. Todo ello no hace sino gatillar un bucle según el cual las células hepáticas comienzan a producir más ácidos biliares en respuesta a la pérdida de los mismos a través de la excreción (tratamos de reponer lo que perdemos). Considerando que los ácidos biliares se forman en el hígado a partir del colesterol, y habida cuenta de la necesidad de reposición de las mismas, el hígado responde sintetizando más ácidos biliares, esta vez a expensas del colesterol circulante y no del primario –ya agotado– lo que disminuye las concentraciones plasmáticas del mismo. Asimismo, al existir menos ácidos biliares, el colesterol atrapado por los geles viscosos avanza hasta alcanzar el ciego, donde una vez liberado tras la fermentación de la fibra ya no supone ningún riesgo, ya que la capacidad de absorción del colon es prácticamente nula. Otro actor de gran importancia en la reducción de la colesterolemia es uno de los ácidos grasos de cadena corta resultantes de la fermentación colónica: el propionato. Sabemos que la enzima que regula la biosíntesis de colesterol hepático es la beta-hidroxi-beta-metil-glutaril CoA reductasa. Sin embargo, se ha demostrado cómo el propionato, toda vez que accede a la circulación portal, inhibe esta enzima, con la consiguiente disminución de la síntesis de colesterol hepático. Así las cosas, vemos cómo la fibra no sólo facilita la eliminación del colesterol circulante, sino que afecta también a su capacidad de biosíntesis. Es precisamente al socaire de esta disminución en los niveles plasmáticos de colesterol en su fracción de LDL de la que deriva otra de las virtudes profilácticas de la fibra dietética: la prevención de la enfermedad cardiovascular. Muchos son los factores implicados en la aparición de la enfermedad cardiovascular, como la edad, genética, hipertensión arterial, obesidad, tabaquismo, altas concentraciones de colesterol, etc. Sin embargo, aun sabiendo que algunos factores de riesgo como la edad y la propia genética quedan por encima de nuestra propia voluntad, otros son única y exclusivamente fruto de nuestros excesos, en unos casos, y defectos, en otros tantos. En el caso que nos ocupa, y como señalamos anteriormente, sabemos cómo actúa la fibra dietética soluble en relación a la disminución de la colesterolemia. Obviando que la enfermedad cardiovascular presenta un origen multifactorial, es de prever que un descenso de los niveles de lipoproteínas de baja densidad incidirá positivamente en lo que a la reducción de riesgos de fallo cardiovascular se refiere. En efecto, diversos estudios epidemiológicos así lo demuestran. El primero de los estudio prospectivos realizados en relación a la ingesta de fibra y la prevención de enfermedad coronaria se llevó a cabo en 1977 por Morris et al. sobre un total de 337 hombres controlados durante 20 años, hallando una relación inversa entre la ingesta de fibra y la morbimortalidad por enfermedad coronaria. Desde entonces, son muchos los estudios realizados, hallando la mayoría de ellos una reducción en el riesgo de enfermedad coronaria que oscila entre el 40-48% cuando comparamos el consumo más alto de fibra (entre 23 y 29 gramos por día) y el más bajo (entre 11,5 y 12,5 gramos por día). Entre los distintos tipos de fibra evaluadas, la mayor respuesta en relación al descenso en el riesgo de enfermedad coronaria se halló siempre vinculada a la fibra soluble, especialmente cereales, disminuyendo ésta un 29% por cada 10 gramos de incremento en el consumo diario. Por si fuera poco, el Estudio de Prevención de la Aterosclerosis de Los Angeles, del año 2003, estableció que una dieta rica en fibra soluble reducía el engrosamiento de la íntima –la capa más interna de los vasos que contacta directamente con la sangre– de la arteria carótida, siendo éste uno de los parámetros indicadores del avance de la aterosclerosis. Finalmente, respecto al factor hipoglucemiante y prevención de la diabetes, sabemos que las fibras viscosas ingeridas en cantidades de entre 10 y 25 gramos por comida disminuyen la respuesta pospandrial de glucemia e insulinemia, como acreditan diversos estudios con pacientes diabéticos no insulinodependientes. En un estudio aleatorio cruzado llevado a cabo por Peterson DB et al. "Low dose guar in novel food product: improved metabolic control in non-insulin-dependent diabetes", donde administraron durante tres periodos de seis semanas pan control (pan normal), pan de guar y pan con granulado de guar, los pacientes que ingirieron pan de guar y pan de granulado de guar, a diferencia de los de control, hallaron reducciones significativas en las pruebas de hemoglobina glicosilada (11,5 a 10,7 en el caso pan de guar y 11,2 a 10,6 en el caso del granulado de guar) sin alterar otro tipo de parámetros y con unas ingestas diarias de 7,6 gramos de guar en el caso del pan de guar y 8,3 gramos en el caso del pan de granulado. Chandalia et al., por su parte, llevó a cabo un ensayo aleatorio y cruzado en el cual administraron durante seis semanas una dieta rica en fibra (50 gramos por día) frente a otra que contenía 24 gramos, hallando un descenso en la glucemia prepandial de un 8,9% en el caso de la dieta alta en fibra.
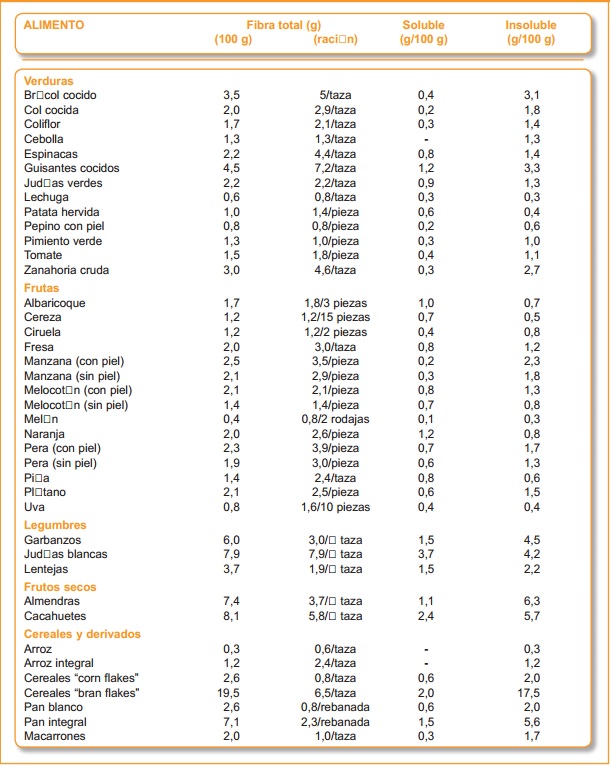
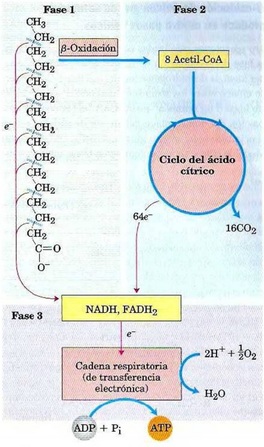
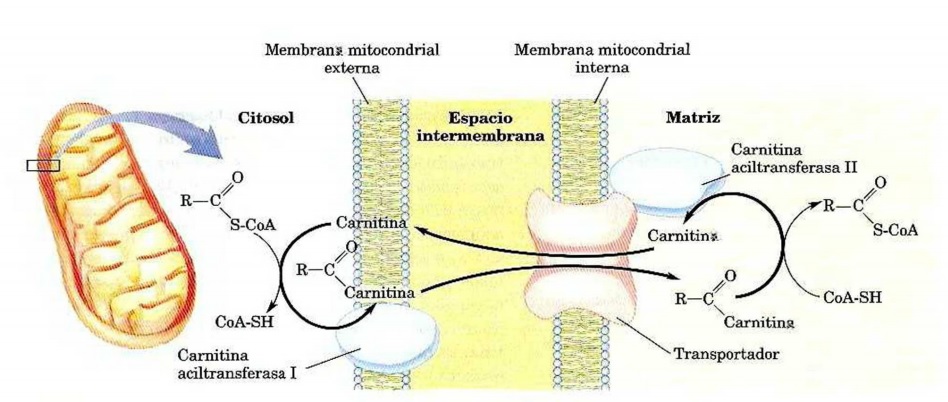
Pero como toda solana esconde su umbría, no todo podían ser virtudes en lo que a la fibra dietética se refiere. Elementos potencialmente adversos presenta y uno muy por encima del resto, ya que las consecuencias derivadas de éste pueden ser la antesala de numerosas complicaciones. Así, sabemos que uno de los efectos de la fibra dietética es el aumento de la masa fecal y velocidad de tránsito. Este incremento en la velocidad obstaculiza la mayor absorción de nutrientes, especialmente de minerales, que junto con la implicación de los fitatos, incide en la reducción de la biodisponibilidad de los minerales propios de los vegetales, siendo éste uno de los puntos negros de las dietas vegetarianas. Y es que manejar los antagonismos entre según qué alimentos no es empresa fácil, tal y como ocurre –pongamos por caso– con la relación entre la vitamina C y la absorción del hierro no hemo, de tal modo que dicha absorción únicamente contrarresta el efecto de los fitatos cuando es ingerida simultáneamente con los alimentos ricos en hierro. Un punto que podemos presuponer que no todos los vegetarianos sin el asesoramiento oportuno serán capaz de manejar con criterios científicos –por no decir la inmensa mayoría–. Igualmente peligroso para los veganos estrictos resulta ser la escasa o nula biodisponibilidad del calcio de los alimentos ricos en oxalato, como así ocurre con las espinacas, acelgas, berros o cacao, todos ellos grandes reservorios de calcio pero de muy escasa biodisponibilidad. Un problema que encontramos también respecto al zinc o el hierro, produciéndose una merma en su biodisponibilidad toda vez que convergen con los taninos y polifenoles. De ahí los numerosos estudios que encuentren menores niveles de hemoglobina o ferritina en los vegetarianos que en omnívoros. Por tanto, vemos cómo una ingesta desmedida de vegetales y, por tanto, fitatos, puede acarrear graves consecuencias, una vez que damos por buena la máxima de que a mayores cantidades, mayores beneficios, ignorando que cuando de fenómenos bioquímicos hablamos, no siempre dos más dos son cuatro. De hecho, el reto de la ciencia de la nutrición es perfilar los límites a partir de los cuales lo beneficioso demuda en nocivo. En el caso de la fibra dietética, se sugiere una ingesta en adultos de entre 20 y 30 gramos por día (25% soluble y 75% insoluble) o, en relación al contenido calórico, de 10 a 13 gramos por cada 1.000 calorías. Con estos mimbres, podemos concluir que existe evidencia científica más que suficiente para ensalzar las virtudes de la fibra dietética, sin que ello la convierta en el mismísimo Bálsamo de Fierabrás. Debemos tener en cuenta que los estudios realizados hasta la fecha encuentran diferentes beneficios adicionales del orden del 1% en cuanto al descenso de la hemoglobina glicosilada o entre el 5-10% en el caso de la colesterolemia. Con todo, al tratarse la hipercolesterolemia como la hiperinsulinemia de elementos etiopatogénicos propios de enfermedades de naturaleza multifactorial, garantizar el control de algunas de estas variables puede marcar la diferencia entre el desencadenamiento de la enfermedad o su prevención. Es importante consignar que las fibras dietéticas, al presentarse en alimentos ricos en antioxidantes y fitoquímicos, resulta difícil establecer hasta dónde llegan los beneficios de éstos y hasta dónde los de la fibra propiamente dicha. De ahí que los ensayos traten de controlar rigurosamente el mayor número de variables posibles. Otro dato importante derivado de estos estudios es la cantidad de puertas que nos abre de cara al desarrollo de futuros fármacos. Especialmente interesantes son todos los resultados obtenidos hasta la fecha en relación a la prevención de determinados tipos de cáncer, aunque en el caso analizado se trate más bien de una concatenación de distintos fenómenos bioquímicos junto a otros estrictamente físicos, como el derivado de una menor exposición de los agentes cancerígenos en el intestino por el aumento de la velocidad del tránsito. Hablamos, por tanto, de un órgano –el intestino– con una superficie de absorción de alrededor de 200 metros cuadrados –poco menos que una cancha de baloncesto– lo que evidencia la complejidad de toda la fenomenología subterránea concerniente a la absorción de los alimentos y lo que de la misma se deriva. De ahí que pequen por igual quienes desprecien las pequeñas mejorías halladas en términos porcentuales como quienes vean en la fibra vegetal un elemento más propio de la chamanería que de la profilaxis dietética. Los hechos son los hechos. Y las opiniones, opiniones. Con todo, podemos barruntar que la fibra dietética seguirá siendo por mucho tiempo esa gran olvidada. Entre los muchos suplementos dietéticos de moda, unos de los más reclamados en estos últimos tiempos son los conocidos como fat-burners o quemagrasas. Estos compuestos, los cuales basan sus supuestos beneficios en las virtudes de la L-Carnitina, ensalzan de un modo bastante ostentoso su capacidad para acelerar el catabolismo de los ácidos grasos en las mitocondrias. Victory Neo Fat Burner Thermoactive; Lipotropic Fat Burner; Nutrisport Fat Burners; o la más discreta L-Carnitina 1500 de la española Santiveri, son sólo una muestra de los miles de complementos de L-Carnitina anunciados en gimnasios, tiendas de dietética y herbolarios. Con todo, estando la L-Carnitina implicada realmente en el catabolismo de los ácidos grasos, ¿podemos afirmar cabalmente que una mayor ingesta de la misma incide proporcionalmente en un aumento en la beta-oxidación de los ácidos grasos? El marketing responde sí cuando la ciencia nos dice con rotundidad que no. Desde los hallazgos de Albert Lehninger en 1948, sabemos que las enzimas implicadas en la oxidación de los ácidos grasos en las células animales se encuentran en la matriz mitocondrial. Por su parte, estos ácidos grasos no difunden libremente a través de las membranas mitocondriales, sino que existe un peaje a cubrir por determinados tipos de ácidos grasos. Los ácidos grasos de menos de doce átomos de carbono entran libremente en la mitocondria sin necesidad de transportadores de membrana. Sin embargo, aquellos otros con catorce o más átomos de carbono –la inmensa mayoría de los ácidos grasos de la dieta o los liberados del tejido adiposo– precisan de lo que conocemos como la lanzadera de la carnitina, una suerte de puente entre el citosol y la matriz mitocondrial. Para cruzar el puente, primeramente estos ácidos grasos de catorce o más carbonos necesitan ser desgajados en piezas más pequeñas de dos átomos de carbono (Acil-Coa) para poder ser oxidados en el interior de la mitocondria. Por ejemplo, el ácido palmítico de dieciséis carbonos da ocho grupos acetilo de dos carbonos que entrarán en la beta-oxidación en una secuencia oxidativa de siete ciclos. Sin embargo, y como hemos señalado anteriormente, la entrada de este ácido graso ya fragmentado no es libre, sino que sucede en tres pasos, mediado cada uno de ellos por un complejo enzimático diferente. La razón por la cual estos ácidos grasos necesitan de un sistema de transporte alternativo es que la membrana mitocondrial interna resulta ser impermeable al paso del Coenzima A del Acil-CoA. Para salvar este obstáculo, el grupo acilo se une temporalmente a la carnitina para dar acilcarnitina. Es como si el grupo acilo del Acil-CoA, menor de edad, necesitara de la presencia de un adulto, la carnitina, para acceder al interior de la mitocondria. Así, una vez formada la acilcarnitina gracias a la carnitina aciltransferasa I (en la cara citosólica de la mitocondria) el grupo acilo y la carnitina acceden de la mano a la matriz mitocondrial mediante la acción de una translocasa que actúa como transbordador entre la membrana externa y la interna. Una vez dentro, el grupo acilo y la carnitina se escinden, de modo que el primero se une a un Coenzima A de la matriz mitocondrial para dar de nuevo Acil-CoA, la misma molécula que no pudo atravesar el espacio intermembrana por la impermeabilidad de la membrana. Por su parte, la carnitina –el adulto– que trajo consigo al interior de la mitocondria al grupo acilo –el menor–, vuelve a la membrana externa para traer al resto de grupos acilo a la matriz mitocondrial. Este proceso se repite hasta que todos los "menores" estén dentro. Así, el proceso de entrada en el que interviene la carnitina se convierte en el paso limitante de la velocidad de la oxidación de ácidos grasos en la mitocondria, siendo, por tanto, un punto de regulación. No obstante, la carnitina aciltransferasa I es inhibida por el manolil-CoA, el primer intermediario de la síntesis de ácidos grasos, de modo que esta inhibición evita que síntesis y degradación se simultaneen.
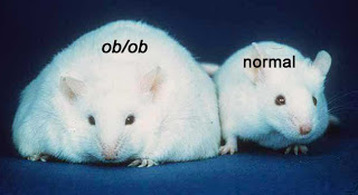
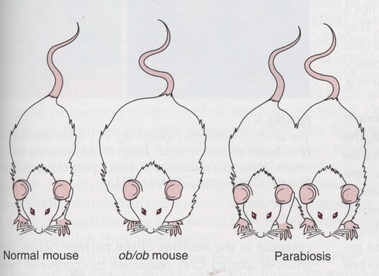
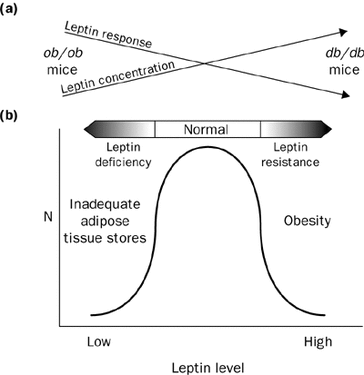
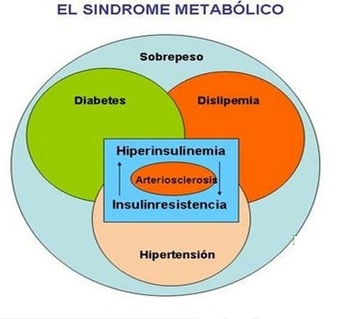
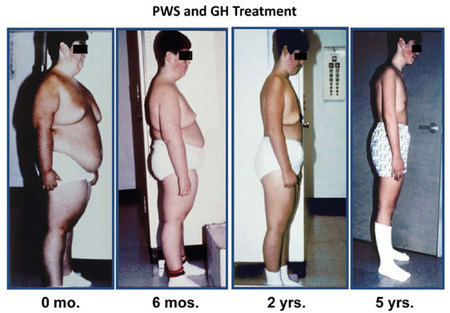
Una vez visto el papel de la carnitina a la hora de facilitar la entrada de los Acil-CoA en la mitocondria a fin de acceder a la beta-oxidación propiamente dicha, cabría preguntarse por qué un mayor aporte de carnitina no aceleraría la oxidación de ácidos grasos prometida por los complementos de L-Carnitina. La razón es muy simple: de igual que el oxalacetato en el Ciclo de Krebs, la carnitina actúa como una de esas puertas giratorias. La misma que entra, sale para volver a entrar, siempre como acilcarnitina. Es decir, actúa cíclicamente. Con todo, ¿sintetizamos toda la carnitina necesaria? ¿Nos basta? ¿Qué ocurriría si añadiésemos mayores cantidades? Tal y como ocurre con las vitaminas hidrosolubles, si nos excedemos, dicho exceso será excretado. Por tanto, añadir a la dieta complementos de L-Carnitina es una buena manera de tirar el dinero al urinario, no alegórica, sino literalmente, ya que la L-Carnitina de más acabará yéndose con la orina sin haber participado en la lanzadera de la carnitina. Y es que de igual que no por tener más lápices al alcance de la mano escribiremos más, no por tener presente más carnitina aceleraremos la oxidación de los ácidos grasos. Pero, ¿y si no sintetizamos la suficiente? Empresa más que improbable esta, habida cuenta que la carnitina se sintetiza ya en exceso en hígados y riñones a partir de la lisina (cereales y legumbres) y metionina (carne, pescado, huevos y lácteos) por lo que cualquier persona con una dieta medianamente equilibrada mantendrá óptima su capacidad de biosíntesis. De hecho, el déficit de L-Carnitina es una enfermedad metabólica extremadamente rara, distinguiéndose entre déficit primario o miopático y déficit sistémico. Por otro lado, los supuestos beneficios de la L-Carnitina alcanzan también a la práctica deportiva a tenor de lo propagado por revistas y webs de culturismo, gimnasios, así como tiendas de suplementación dietética. Un hecho que, pese a no contar con ningún tipo de evidencia científica concluyente, ventean con pomposidad como hecho experimentalmente probado. No obstante, hace apenas dos años, en junio de 2011, la Agencia de Seguridad Alimentaria Europea (EFSA) concluyó tajantemente que «una relación de causa y efecto no se ha establecido entre el consumo de L-carnitina y la recuperación más rápida de la fatiga muscular del ejercicio, la reparación del tejido muscular esquelético y el aumento de la capacidad de resistencia». Un hecho que poco o nada importa a una industria –la de los suplementos dietéticos de gimnasios y herbolarios– que desde sus orígenes viene desoyendo cualquier tipo de recomendación e incluso reglamentación, habida cuenta de su status de privilegio según el cual no precisan respaldar sus productos con evidencias científicas que acrediten no sólo su inocuidad, sino además sus efectos farmacológicos, así como contraindicaciones, antagonismos, efectos sinérgicos, etc. Con todo, lo cierto es que tras más de medio siglo de estudio de la L-Carnitina, nada de lo prometido por los cientos de fabricantes de suplementos dietéticos encuentra andamio alguno sobre el que sustentarse, salvo el del fraude más desacomplejado. Y es que, como sentenciara Talleyrand, «lo que no puede ser, no puede ser, y además es imposible». Máxime cuando hablamos de algo tan complejo y riguroso como la bioquímica. Otra cosa muy distinta es que por dinero sean capaces de hacer de lo imposible un probable, hasta el punto de vendernos los milagros de la misma purga de Benito. Cuando en 1949 se halló casualmente el primer ratón ob/ob en una colonia del Jackson Laboratory, muchos científicos vieron en el mismo la auténtica Piedra de Rosetta a partir de la cual se engarzarían todas las piezas conocidas hasta la fecha respecto al inmenso puzle de la obesidad. Más si cabe cuando años más tarde, en 1994, el genetista molecular Jeffrey Friedman, del Instituto Médico Howard Hughes de la Universidad de Rockefeller, consiguió aislar el producto del gen OB (obeso) en ratones de laboratorio: la leptina. Los ratones portadores del genotipo ob/ob (las dos minúsculas indican que presentan dos copias mutantes del gen OB) resultaron ser fenotípicamente iguales que el resto de ratones, con la particularidad de que comenzaban a aumentar de peso al poco tiempo hasta triplicarlo. Es decir, los ratones ob/ob mostraban el comportamiento propio de un animal en ayuno: niveles plasmáticos de cortisol elevados, desequilibrios en la homeostasis térmica, crecimiento anormal, incapacidad para la reproducción y un apetito voraz. Además, presentaban desarreglos metabólicos propios de la diabetes, incluyendo la resistencia a la insulina. De igual que las dos copias mutantes ob/ob inducían la aparición de lo que conocemos como obesidad genética, los científicos hallaron también las dos copias mutantes del gen DB (diabetes) db/db, encargado de codificar el receptor de la leptina en el núcleo arcuato del hipotálamo, de tal forma que los animales con las dos copias mutantes daban ratones diabéticos, obesos y resistentes a la leptina. En cuanto a la leptina propiamente dicha, sabemos a través de las observaciones de Friedman que se trata de una hormona peptídica de 167 aminoácidos, con una secuencia de 21 aminoácidos que se escinde antes de pasar al torrente sanguíneo. Por lo tanto, la hormona ya activa y madura presenta una secuencia de 146 aminoácidos. Perteneciente al grupo de hormonas anorexigénicas, se encarga de la regulación del apetito y la ingesta de alimentos, al igual que la colecistocinina, bombesina o amilina. Al actuar sobre las neuronas anorexigénicas del núcleo arcuato del hipotálamo, libera la hormona estimulante de los alfa-melanocitos (alfa-MSH) que hace que la siguiente neurona del circuito envíe al cerebro la señal de saciedad. Producida por los adipocitos y, en menor medida, por la mucosa del fundus gástrico, su concentración depende de la cantidad de tejido adiposo que presente el individuo, de modo que las concentraciones séricas en individuos obesos pueden sobrepasar los 30 ng/ml, mientras que en individuos con normopeso oscila entre los 1-15 ng/ml, manteniendo una vida media en suero de alrededor de los 25 minutos. En relación a los ratones ob/ob y su incapacidad de codificar su producto (leptina) los investigadores administraron la hormona purificada diariamente a los ratones con defectos en el gen OB a fin de estudiar su respuesta. Los resultados fueron asombrosos: ratones de 67 gr alcanzaron un peso de 35 gr. Además de la pérdida ponderal, los ratones aumentaron la actividad locomotora y termogénesis, con el consiguiente aumento del gasto energético. Un fenómeno que explicaría por qué al unir quirúrgicamente dos ratones (parabiosis), uno genéticamente obeso junto a otro normal, el primero acababa por reducir su peso mientras que el segundo no, toda vez que ambos comenzaban a compartir el mismo aparato circulatorio y, con él, el factor saciante de la leptina transmitido por la sangre del animal sano. Respecto a los humanos, una vez identificado y aislado su propio gen OB, con un locus cromosómico 7q31-3 (el 7 indica el cromosoma en cuestión; q de brazo largo, en contraposición a la p de brazo pequeño; y 31-3 de banda 3, sub-banda 1 y sub-sub-banda 3) los científicos realizaron las mismas pruebas experimentales, logrando idénticos resultados a los obtenidos en ratones. Tras administrar leptina recombinante sobre determinados individuos obesos, éstos hallaron una relación dosis-respuesta entre la pérdida ponderal y la inyección de leptina. Todo ello aplicado sobre individuos con el gen OB mutado. Sin embargo, la cruz de la moneda es que, por desgracia, esto apenas representa el 10% de los casos de obesidad mórbida, ya que sabemos que, paradójicamente, en la inmensa mayoría de individuos obesos el gen OB permanece intacto y, por tanto, su capacidad de producir leptina se mantiene inalterada. No obstante, todo lo hallado hasta el momento parece darnos las coordenadas correctas hacia dónde dirigirnos en relación al papel jugado por la leptina respecto al modelo lipostático. Así las cosas, sabiendo que los niveles de leptina en sangre son mucho más elevados en individuos obesos que en aquellos otros con una masa corporal normal, podríamos pensar que, al igual que ocurre con la insulina en la diabetes, se trataría más bien de una falla en el uso que el propio organismo hace de la hormona y el rendimiento que obtiene de ésta, así como deficiencias en los receptores de leptina y la propia resistencia a la misma. Uno de los puntos de entibación de esta teoría nos lo ofrece la observación por radioinmunoanálisis de las concentraciones de leptina en el líquido cefalorraquídeo (LCR) en comparación con las concentraciones séricas. Mediante esta técnica de análisis, en la que se utilizan isótopos radiactivos para cuantificar de un modo exacto las mínimas señales hormonales, se observa de qué manera las concentraciones de leptina en el líquido cefalorraquídeo son más bajas que las concentraciones séricas, lo que evidenciaría una alteración del transporte de la leptina a través de la barrera hematoencefálica en los individuos obesos, tal y como señala Michael W. Schwartz, del Departamento de Medicina de la Universidad de Washington, en su trabajo publicado en la revista Nature: Central Nervous System control of food intake Por otro lado, sabemos que entre la leptina y la insulina existe una perfecta homeostasis, de tal modo que la leptina inhibe la secreción de insulina por parte de las células beta pancreáticas, mientras que la insulina estimula la síntesis de leptina en el adipocito. Sin embargo, bajo determinadas circunstancias esta homeostasis acaba por desgajararse. Durante la patogénesis de la diabetes mellitus de tipo 2 tiene lugar lo que conocemos como la curva de Starling del páncreas. Según la misma, se hilan una serie de pasos mediante los cuales el individuo pasa lentamente de un estado de normoglucemia con normoinsulinemia a otro de intolerancia a la glucosa con hiperinsulinemia (previa resistencia insulínica) para acabar en el punto de hipoinsulinemia por agotamiento pancreático. Es decir, las células beta quedan literalmente exangües por el sobreesfuerzo realizado durante años hasta perder su capacidad de biosíntesis. Por otra parte, tratándose la leptina de la hormona de la saciedad, ¿cómo es posible que determinados individuos obesos sean incapaces de atender a dichas señales aun sabiendo que presentan mayores concentraciones plasmáticas de la misma? La respuesta parece hallarse muy en sintonía con lo descrito en relación a la curva de Starling del páncreas. Es decir, existen más que indicios para sospechar que determinados individuos obesos alcanzan un estado de resistencia a la leptina del mismo modo que el prediabético alcanza su estado de resistencia a la insulina: por sobreexposición a la hormona. De este modo, tenemos individuos ya obesos con altos niveles de leptina pero completamente sordos a las señales neuronales de detención de la ingesta calórica por resistencia a la leptina, así como individuos que presentan una deficiencia de leptina que acaba por provocar una obesidad severa por hiperfagia persistente pese a los altos niveles de insulina. Todo ello dejando claro el papel predominante de la leptina frente a la insulina en el control de la homeostasis de la energía en el SNC, aun siendo ambas hormonas proporcionales al contenido de tejido graso. Por otro lado, trabajos como los realizados por William J. Whelan, del Departamento de Bioquímica y Biología Molecular de la Universidad de Miami, demostraron cómo determinados alimentos como aquellos ricos en fructosa –de la que hablaremos otro día por sus desastrosos efectos sobre el organismo– acaban por inducir no solo hipertrofia cardiaca, alto colesterol, diabetes de tipo 2 o esteatosis hepática, sino que además crea grandes alteraciones en el balance entre leptina y grelina (hormona orexigénica liberadora del neuropéptido-Y que envía la señal de hambre) aumentando la concentración de ésta última. Sabiendo, además, que en Estados Unidos llegaron a identificar a la fructosa en más de 600.000 productos alimenticios en su forma de jarabe de maíz de alta fructosa, incluidos muchos de los alimentos aptos para diabéticos dada su lenta liberación de glucosa, la relación entre dieta, obesidad y resistencia a la leptina –muy posiblemente en este mismo orden– parece hacerse cada vez más estrecha si cabe, así como su incidencia en el alarmante aumento de casos de Síndrome Metabólico. Todo ello obviando que no todos los tipos de obesidad presentan la misma naturaliza y origen, especialmente aquellos casos de obesidad genética, como la que encontramos en el Síndrome de Bardet-Biedl o el Síndrome de Prader-Willi, siendo éste último una de las causas de obesidad genética más frecuentes, con pacientes que llegan a alcanzar los 100 kg de peso con tan solo 10 años de edad por un déficit en la producción de leptina y un incremento en la liberación de grelina, presentando hiperfagia y ausencia de saciedad, con una continua y constante ingesta calórica sin curva de desaceleración. Unos efectos derivados de la enfermedad que, por suerte, a día de hoy pueden ser minimizados gracias al tratamiento hormonal. De este modo, tratándose la obesidad de una enfermedad que afecta a una tercera parte de la población adulta en los países industrializados y con una incidencia en ciernes entre la población infantil, especialmente en nuestro país, donde desde 2011 superamos a Estados Unidos con un 19% de obesidad entre nuestros menores, la comprensión de toda esa maquinaria subterránea de la enfermedad –aquella ajena a las causas externas como las culturales– se antoja no sólo necesario, sino imprescindible. Más si cabe a la hora de minimizar el enorme coste psicológico y emocional de aquellos pacientes obesos para los que la obesidad, en general, y la hiperfagia, en particular, representan un auténtico estigma social que no hace sino aumentar los sufrimientos derivados de la enfermedad.
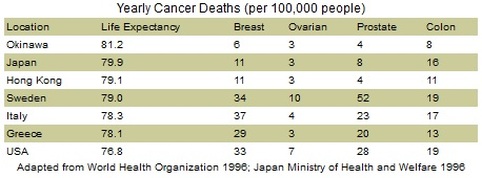
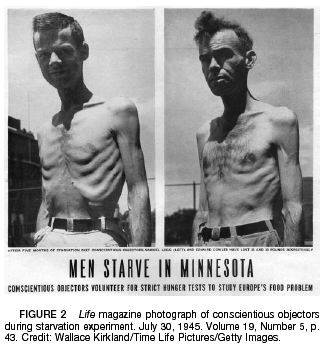
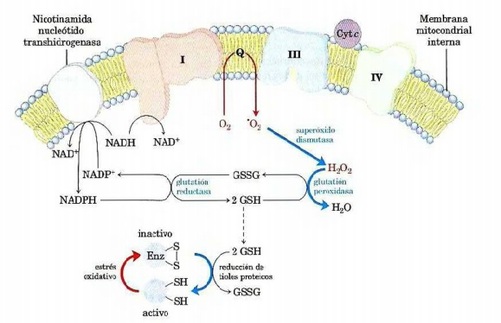
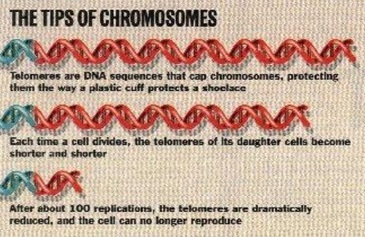
El estudio de la leptina y su efecto sobre las neuronas anorexigénicas nos brinda una visión más amplia si cabe respecto a los mecanismos de retroalimentación del modelo lipostático y la acción reguladora de la hormona, así como el aumento en la termogénesis dado su papel en el desacoplamiento entre el transporte de electrones de la cadena electrónico mitocondrial y la síntesis de ATP en las mitocondrias de los adipocitos. Por tanto, de igual que el humo nos lleva al fuego, los distintos avances en el estudio de la leptina parecen conducirnos al lugar preciso donde tiene lugar el punto de ignición mismo de determinados tipos de obesidad. «Hara hachi bu». O lo que es lo mismo: estómago lleno ocho partes de diez. Así reza el famoso mantra confuciano por el cual vienen rigiéndose los habitantes de la Isla de Okinawa a la hora de enfrentarse a sus frugales comidas diarias. Un 80% de su capacidad de ingesta total. Es posible que los okinawenses representen la única comunidad del mundo sometida voluntariamente a lo que conocemos como restricción calórica (RC). Y ésta, aun perfilando los límites del 20%, no desmerece en fondo y forma a lo que a través de tal práctica es posible alcanzar. Conocida por vieja es la relación entre comer menos y vivir más, siempre que esta merma en la ingesta no represente desequilibrios en las proporciones nutricionales. Es decir, se trataría de ingerir la misma proporción de principios inmediatos que en una dieta estandarizada pero en dosis inferiores. En Okinawa se concentra la mayor densidad de población centenaria del planeta. Además, determinadas enfermedades propias de la civilización occidental brillan por su ausencia. Este hecho, en un paroxismo de burdo atrevimiento, podría achacarse a la propia genética de los okinawenses, de modo que en la lotería de la evolución sus boletos resultaran premiados y, a quien Dios se la dé, San Pedro se la bendiga. Sin embargo, los hechos son muy otros. En un estudio descriptivo realizado sobre 100.000 okinawenses emigrantes residentes en Brasil y los cuales adoptaron los hábitos alimenticios propios del país, la esperanza de vida se vio reducida en 17 años respecto a sus iguales residentes en la Isla de Okinawa. Idénticos resultados fueron hallados en los distintos estudios de poblaciones llevados a cabo con los japoneses residentes en Hawai y California, toda vez que éstos asumieron la Western diet. Todo esto no hace sino descartar el factor genético, ya que la incidencia de ciertas enfermedades como la cardiopatía isquémica o determinados tipos de cáncer (ver tabla), varía según el lugar de residencia. No obstante, lo que conocemos hasta el momento en relación a la restricción calórica en humanos presenta multitud de aristas. Mucho de lo que sabemos acerca de la influencia de la restricción calórica sobre el envejecimiento proviene de los estudios clásicos de McCay et al. llevados a cabo durante los años 30 del siglo XX. Durante los mismos, el equipo de McCay demostró que las ratas sometidas a restricción calórica tenían una esperanza de vida superior en un 33% al grupo control. Sin embargo, su tamaño y maduración aparecían notablemente atrofiados. Años después se adheriría a la causa el prestigioso fisiólogo norteamericano Ancel Keys –a quien en esta orilla recordamos por ser el partero de la «dieta mediterránea»–. Los resultados del Experimento de Minnesota, como así se le conoció a dicho estudio, fueron cuanto menos turbios, ya que lo que se logró fue un estado de inanición controlada en la que tanto los cambios físicos como cognitivos fueron visibles. Durante el experimento, se sometió a un grupo de objetores de conciencia de la Segunda Guerra Mundial a una restricción calórica del 50% durante once meses, mediante la cual alcanzaron una pérdida ponderal del 25% respecto al peso inicial, con sus correspondientes derivados fisiológicos. Pero si hay algo que llamó la atención, fue el daño emocional sufrido por los sujetos experimentales: trastornos de la personalidad, depresión, períodos de elación seguidos de apatía, deterioro del cuidado de la higiene, ansiedad, así como desórdenes psicóticos, fueron muchos de los males comunes a los participantes durante los meses que duró el experimento e incluso mucho después del mismo. Huelga señalar a modo de macabra anécdota que, por una de esas ironías de la historia, ni el propio Keys ni los voluntarios implicados sabían en ese momento que lo conseguido en el Experimento de Minnesota se estaba ya logrando en los campos de concentración de Dachau, Majdanek o Treblinka de uno modo mucho menos ortodoxo. Cuando hablamos de los okinawenses, hacemos referencia a un proceso cultural mediante el cual logran, a lo sumo, un desfase en el aporte calórico del 20%. Con todo, se estima que la ingesta calórica media de los habitantes de Okinawa pendula entre las 1500-1800 calorías diarias. Nada alarmante, habida cuenta de las 2000 calorías diarias recomendadas por la USDA. Por lo tanto, en lo sucesivo, hablaremos de restricción calórica en un sentido mucho más riguroso: 40-50%. Lo que nos dice el estudio acerca de la restricción calórica en animales es bastante revelador, no en vistas a implementar restricciones del 40-50% en seres humanos, sino a lo que vamos conociendo respecto a los mecanismos celulares implicados en el proceso de envejecimiento. Y es que las huellas filogenéticas de nuestros predecesores se solapan entre sí, de modo que sabemos que los mecanismos capaces de hilar restricción calórica y longevidad se mantienen parejos entre los distintos organismos estudiados, desde levaduras, nematodos, moscas, peces, roedores hasta, finalmente, nuestros parientes más cercanos: los monos. Es por ello por lo que existen razones más que sólidas para relacionar restricción calórica y longevidad incluso entre los seres humanos. A día de hoy, son dos las teorías más ampliamente aceptadas en la explicación de los mecanismos del envejecimiento, íntimamente interconectadas entre sí: la teoría de la glucosilación no enzimática de proteínas y la teoría de los radicales libres. Respecto a la teoría de la glucosilación no enzimática de proteínas –también conocida como reacción de Maillard– sabemos que está más que presente en cada una de nuestras cocinas, ya que es ésta la reacción por la cual determinados alimentos adquieren ese color parduzco o café cuando son calentados en exceso, ya se trate de una parrillada o del caramelo tostado. Bioquímicamente hablando, significa que el grupo amino de las proteínas reacciona con el grupo carbonilo de los azúcares, formando un compuesto intermedio llamado base de Schiff y que, mediante una serie de complejas biotransformaciones, formará los productos de glucosilación avanzada. Entre las enzimas estudiadas sobre las cuales la acción de los productos de glucosilación avanzada incide en la disminución de su actividad biológica, reseñaremos dos: la bomba de calcio (Ca2+ATPasa) y la superóxido dismutasa (SOD), actriz principal ésta última de la teoría de los radicales libres. La bomba de calcio juega un papel esencial en la regulación de la concentración citoplasmática del catión calcio (especialmente en el eritrocito), de modo que su inactivación por los productos de glucosilación avanzada genera grandes alteraciones en la expresión génica, diferenciación celular y determinadas funciones neuronales, entre otras muchas más. En cuanto a la superóxido dismutasa, sabemos que, junto con la catalasa, representan las joyas de la corona de los antioxidantes. Todos los pasos oxidativos de la degradación de glúcidos, grasas y aminoácidos convergen en la cadena de transporte electrónico mitocondrial y fosforilación oxidativa. Durante la reducción del oxígeno a agua en el último paso de la cadena de transporte de electrones, a menudo sucede que se produce una reducción parcial o incompleta del oxígeno, dando lugar a moléculas muy reactivas que conocemos como radicales libres. Estos radicales libres (peróxido de hidrógeno, superóxido y oxígeno singlete) poseen un electrón sin aparear, por lo que crean reacciones en cadena, generando un efecto dominó mediante el cual se desestabilizan numerosas moléculas de toda naturaleza. Uno de los efectos más nocivos de estas especies reactivas del oxígeno (ROS) es el estrés oxidativo, responsable directo de la muerte celular por apoptosis, envejecimiento celular, cáncer, mutaciones, etc. Este es, por tanto, el andamiaje sobre el que descansa, a fin de cuentas, la teoría del envejecimiento. Y esta es la razón por la cual una merma en la biosíntesis de agentes antioxidantes como la superóxido dismutasa puede dar lugar a errores y fallos acumulativos tanto en la expresión génica como en la propia salud mitocondrial. Recordemos que las mitocondrias, al carecer de histonas y de mecanismos de reparación, presentan una más que acentuada falta de protección de su genoma mitocondrial, por lo que la destrucción por los radicales libres se torna irreversible Volviendo a lo que nos ocupa, y en relación con la restricción calórica, sabemos que con la misma los pistones de la mitocondria no alcanzan el grado de erosión que cabría esperar con el transcurso de una dieta hipercalórica, ya que el número de electrones que desembarcan en el citocromo c con el fin de reducir el oxígeno a agua es mucho menor, por lo que el riesgo de generar radicales libres ROS es menos elevado. Por tanto, es posible conocer por qué una menor ingesta de calorías está en íntima relación con un menor daño oxidativo; pero, ¿basta tan solo eso para explicar la relación entre longevidad y restricción calórica? De acuerdo con los científicos del Instituto Salk de Estudios Biológicos de San Diego, California, la respuesta se halla un paso más allá y tiene nombre y apellido: PHA-4. Según los hallazgos del equipo de Siler H. Panowski, el gen PHA-4 sería la llave que abriría o cerraría el mayor envejecimiento en relación con la restricción calórica. «Si se bloquea el gen PHA-4, la restricción calórica no produce efecto alguno, mientras que si se incentiva la actividad de este gen se produce un envejecimiento prolongado, armonioso y dinámico», aseveran. Estos hallazgos, logrados tras años de estudios de la restricción calórica en el nematodo Caenorhabditis elegans, hacen barruntar los mismos efectos con la versión humana del gen, el Foxa-1, después de haber obtenido idénticos resultados en los trabajos con el PHA-4 en mamíferos. Lo cierto es que toda vez que lograron sobreexpresar el gen PHA-4 en el Caenorhabditis elegans, éste alcanzó una longevidad 20-30% mayor que el grupo control. Por su parte, el Profesor Leonard Guarente, del departamento de Biología del imponente Instituto Tecnológico de Massachusetts (MIT), halló el modo en que las sirtuinas, enzimas implicadas en la expresión de los genes SIRT-1, SIRT-3 y SIRT-4 (Silent Information Regulator), aumentaban en relación a la restricción calórica. De la SIRT-1 sabemos que inhibe la biosíntesis de insulina, además de ser un modulador de la apoptosis celular, todo ello en base a su acción sobre el gen p53, de la familia de los genes supresores tumorales, lo que explicaría no sólo la mayor longevidad lograda mediante la restricción calórica, sino además, la merma en el desarrollo de tumores en los animales estudiados en comparación con sus iguales de control. Pero si hay alguien que se entromete entre los factores del trinomio restricción calórica, longevidad e inhibición del crecimiento tumoral, son sin duda los telómeros. Los telómeros son los encargados de proteger los extremos de cada uno de nuestros cromosomas, conformando una suerte de caperuza altamente repetitiva que se erosiona con cada una de las divisiones celulares. Es por ello por lo que las células cancerosas acaban por volverse inmortales, ya que la actividad de la telomerasa (enzima encargada de la elongación de los telómeros) se halla incrementada, de modo que no sólo no envejecen ni se erosionan con cada división, sino que pueden dividirse hasta el infinito sin encontrar freno o resistencia alguna. Sin embargo, se ha comprobado experimentalmente cómo animales expuestos a una restricción calórica del 40% presentaron una menor velocidad en la reducción de los telómeros conforme se producían las distintas divisiones celulares, lo que se tradujo en un número menor de aberraciones cromosómicas, tumores, así como un aumento del 20% en la vida media. Todo ello en el plano de la genética, pero ¿qué ocurre con los factores epigenéticos? ¿Acaso no existen elementos negativos en relación a la restricción calórica? Existen y afectan, principalmente, al desarrollo y maduración del cerebro, así como a determinadas funciones. Por lo estudiado hasta el momento, sabemos que ratones expuestos a una restricción calórica del 40% presentaron una disminución en el número de espinas dendríticas de las neuronas piramidales de la corteza, una mielinización deficiente de los axones, así como un mayor incremento de muerte neuronal. Como consecuencia de esto, el efecto de la restricción calórica sobre la capacidad de aprendizaje fue más que evidente. Durante los estudios, sometieron a los roedores al Test de Morris, un procedimiento destinado a evaluar la capacidad de aprendizaje de los ratones y que consiste en registrar el nivel de aprendizaje del animal toda vez que es colocado sobre una piscina cilíndrica con una plataforma sumergida no visible sobre la que el ratón descansará una vez que logre alcanzarla. Durante sucesivos intentos, observaron que los animales alimentados ad libitum presentaban una mayor capacidad de aprendizaje que aquellos otros sobre los cuales se aplicó la restricción calórica. Por el contrario, cuando los animales crecían en un ambiente enriquecido, es decir, con unas muy buenas condiciones de salubridad, ausencia de factores estresantes así como alimentación ad libitum, el número de espinas dendríticas (el auténtico sustrato físico de la memoria donde se registra el mensaje gracias a la excitabilidad inducida por el glutamato) aumentaba considerablemente. Nada de extrañar, habida cuenta de todo lo ya estudiado a nivel cognitivo durante el Experimento de Minnesota y otros. Mucha tinta se ha derramado sobre la viabilidad de la restricción calórica en su sentido más estricto aplicada a humanos. Son muchos los que esperan hallar en la misma una suerte de purga de Benito. Los hechos, por el contrario, la convierten más bien en una herramienta de trabajo enfocada al estudio del envejecimiento y determinados fenómenos biológicos y conductuales según se trate de restricción calórica, alimentación ad libitum, alimentación diaria limitada, alimentación control o ayuno intermitente, tal como se estudió en los famosos estudios de Masoro et al. Lo cierto es que la inviabilidad de la restricción calórica aplicada a humanos tras el destete, como se ha llevado a cabo con animales, es absoluta. Y es que, según los experimentos de Masoro, los ratones estudiados bajo condiciones de restricción calórica del 40% llegaban a crecer el 51% de los ratones alimentados ad libitum. Esto significa que un ser humano adulto criado bajo condiciones de restricción calórica pesaría del orden de 35 kg en lugar de 70 kg del peso normal. Además, conviene no olvidar en relación a esta inviabilidad temprana que determinadas estructuras del organismo humano no completan su desarrollo hasta llegada la edad adulta, tal y como ocurre con la corteza prefrontal, encargada de la función ejecutiva, es decir, la toma de decisiones, regulación de la conducta, establecimiento de juicios morales o la evaluación de acciones futuras con la información presente. Trastornos como la esquizofrenia, sociopatías o trastorno bipolar se hallan relacionados con daños en la corteza prefrontal, por lo que los posibles riesgos serían inasumibles.
Otro punto importante en relación a la longevidad y ausencia de determinadas enfermedades según el tipo de alimentación es el de la manera en la que los principios inmediatos son adquiridos. Está ampliamente documentado cómo la suplementación nutricional con complejos vitamínicos resulta ser mucho más ineficiente, siendo éstos menos biodisponibles que aquellos otros vehiculizados por los propios alimentos. Estudios como el The Heart Outcomes Prevention Evaluation, en el que siguieron durante casi cinco años a 10.000 pacientes bajo riesgo elevado de fallo cardiovascular y a los que suministraron suplementación con magnesio 265 y vitamina E, no encontraron diferencia alguna en la respuesta respecto al grupo al cual se le administró el placebo. De igual cabe señalar lo analizado en un gigantesco estudio realizado en Estados Unidos durante 1982 y 1998 sobre 1.000.000 de enfermos de cáncer de vejiga en su relación con la vitamina C. Por lo tanto, parece importante no sólo el cuánto, sino el cómo. Con todo, se estima que unas 10.000 personas en el mundo se hallan voluntariamente bajo restricción calórica stricto sensu. La dispersión de las mismas, así como la exposición a distintas condiciones ambientales o proporciones nutricionales hacen imposible el estudio de las mismas. Con lo que sí contamos, por el contrario, es con la experiencia de determinadas poblaciones como los okinawenses o los adventistas del Séptimo Día de California, una de las cohortes más numerosas que han sido estudiadas durante periodos más prolongados (más de 300 artículos publicados desde 1960, cuando comenzó el primer estudio) y quienes siguen una dieta semivegetariana, comiendo carne menos de una vez por semana. Un grupo que, en comparación con la población americana, tienen una mortalidad por cardiopatía isquémica, cáncer de pulmón y cáncer de colon muy inferior, además de tener una esperanza de vida nueve años por encima. Así las cosas, una vez que la ciencia vuelca por el desagüe toda posibilidad de implementar la restricción calórica en humanos, sí nos queda en cierto sentido el consuelo de saber que entre Pinto y Valdemoro seguirán existiendo grupos como los abuelos de Okinawa, esos ancianos centenarios que seguirán diciendo con sus sempiternas sonrisas que la clave de su longevidad «no está en lo que comen, sino en lo que no comen». A nosotros, los occidentales, nos tocará la difícil tarea de hallar el punto de equilibrio entre el inmediatismo del placer hedonista y la profilaxis alimentaria. Nadie dijo que fuera del todo imposible en este rabo de Europa por desollar, aun sin aspirar a los 116 años del jovial Jiromeon Kimura, el hombre más anciano de la historia, fallecido en junio de este año. Cómo no, okinawense. «Hara hachi bu». |
| A HOMBROS DE GIGANTES |
|


 Fuente RSS
Fuente RSS

