Fue a comienzos del siglo XVII cuando Gaspare Aselli, médico italiano conocido por sus hallazgos en relación con los vasos linfáticos intestinales o quilíferos, asentó las bases de lo que con el devenir de los años sería la actual ''teoría lipolítica''. Con todo, aún fueron muchas las idas y venidas acontecidas en el arriscado campo de la angiología, en general, y del sistema linfático, en particular, hasta su ulterior confirmación. Tan es así que no fue sino hasta 1856 cuando el fisiólogo francés Claude Bernard consiguió demostrar que los lípidos ingeridos con la dieta acababan alcanzando el sistema linfático. No obstante, el mecanismo según el cual estos lípidos pasaban de la luz intestinal al sistema linfático no pareció quedar del todo claro. Dos mecanismos fueron los propuestos por entonces: por un lado, la hipótesis de Immanuel Munk, según la cual los triacilgliceroles atravesaban íntegramente la mucosa intestinal mediante una emulsión; y por el otro lado, la hipótesis del fisiólogo alemán Eduard Pflüger, al socaire de la cual se llegó a afirmar que los triacilgliceroles de la dieta eran desdoblados en ácidos grasos y glicerol para ser posteriormente absorbidos. Al modelo de Munk se le conoció como la ''teoría particulada'', mientras que al de su coetáneo se le bautizó como la ''teoría lipolítica'', la cual sería confirmada tiempo después al abrigo de los trabajos realizados en relación con la lipasa pancreática y la hidrólisis de los triacilgliceroles como peaje a cubrir para su posterior absorción.
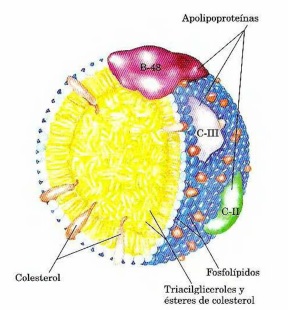
A día de hoy es copiosa y completa la información que poseemos al respecto. Por ejemplo, conocemos el modo en que las grasas de la dieta son emulsionadas por las sales biliares para posteriormente ser hidrolizadas por la lipasa pancreática, atravesar la mucosa intestinal y penetrar en el enterocito, donde los mismos triacilgliceroles antes desdoblados son reunificados de nuevo. Igualmente, sabemos cómo estos triacilgliceroles son encapsulados bajo el paraguas de una capa similar a las membranas biológicas (fosfolípidos, proteínas y colesterol no esterificado) hasta formar los quilomicrones, los cuales acceden a los capilares linfáticos mediante exocitosis para así poner rumbo al sistema circulatorio a través de la vena subclavia izquierda, donde tiene lugar el drenaje (junto a la vena yugular externa). Son estos quilomicrones, repletos de triacilgliceroles y con apoproteínas B-48 varadas en su exterior, quienes evacúan su contenido en las células musculares o tejido adiposo toda vez que la lipoproteína lipasa es activada por el coenzima Apo C-II en el exterior de la célula endotelial (cuyo anclaje impide además el arrastre del quilomicrón por la corriente sanguínea) y así liberar su contenido al citoplasma de la célula en cuestión. Una vez producido el trasvase, los quilomicrones residuales llegan hasta el hígado, donde ceden el colesterol y, finalmente, son degradados en los lisosomas de los hepatocitos.
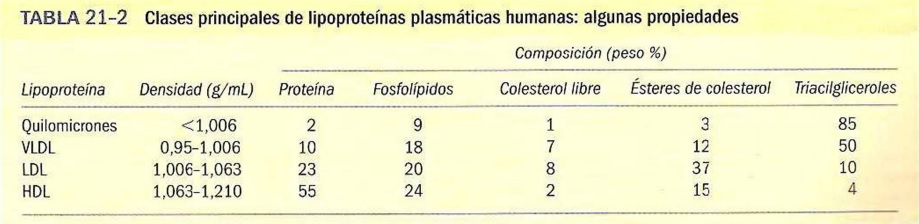
Por el contrario, cuando la dieta aporta más ácidos grasos de los que van a ser requeridos inmediatamente como combustible, el proceso es bien diferente, ya que éstos pasan a formar triacilgliceroles en el hígado, donde se encapsulan formando lo que conocemos como lipoproteínas de muy baja densidad (VLDL), un fenómeno que ocurrirá de igual siempre que la dieta nos aporte grandes cantidades de glúcidos. Estas lipoproteínas, las cuales poseen mayores cantidades de colesterol esterificado, liberan su contenido en ácidos grasos y glicerol tras la activación de la lipoproteína lipasa por la Apo C-II, de tal modo que son captados por el tejido adiposo para su reagrupación en triacilgliceroles, mientras que los miocitos los oxidan para el rendimiento energético. La pérdida progresiva de triacilgliceroles convierte a las VLDL en IDL (lipoproteínas de densidad intermedia o remanentes de VLDL). Una vez que estas IDL continúan liberándose de su contenido en triacilgliceroles, demudan en lo que conocemos como LDL (lipoproteínas de baja densidad) muy ricas en colesterol esterificado, el cual es transportado hasta los tejidos extrahepáticos, toda vez que los receptores específicos de éstos reconocen las apoproteínas B-100 del exterior de las LDL. Con todo, en el mismo hígado tiene lugar la biosínstesis de otro tipo de lipoproteínas y, quizás, las más conocidas: las HDL o lipoproteínas de alta densidad, las cuales realizan una suerte de pesca de arrastre catalizando la formación de ésteres de colesterol a partir de la fosfatildilcolina (remanente de los quilomicrones y las VLDL residuales) y el colesterol, para retornar finalmente al hígado para así descargar el colesterol recuperado y ser transformado en sales biliares.
Evitando ahondar en los complejos procesos bioquímicos implicados en lo relativo a la asimilación, síntesis de colesterol, asimilación y liberación de los ácidos grasos, etc., y considerando todo lo anterior como mero andamiaje sobre el que armar todo lo que comentaremos a continuación, nos centraremos en un tipo de ácido graso muy concreto y las biotransformaciones que éste sufre, así como sus repercusiones metabólicas: los ácidos grasos poliinsaturados.
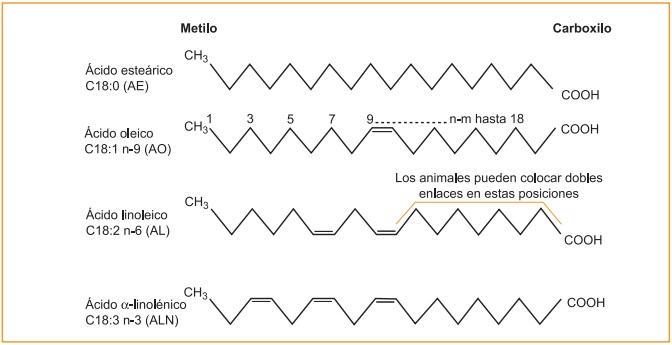
Cuando hablamos de ácidos grasos poliinsaturados, hacemos referencia a un tipo de ácido graso esencial (debe ser aportado en la dieta) que presenta varias insaturaciones; es decir, posee más de un doble enlace carbono-carbono. Huelga señalar que dicha esencialidad se fundamenta en el hecho por el cual los humanos no podemos introducir insaturaciones a partir del carbono situado en la posición novena, partiendo desde el extremo carboxílico hacia el extremo metilo. De ahí nuestra incapacidad a la hora de sintetizar tanto el ácido linoleico [C18:2 n-6 (9,12)] como el ácido linolénico [C18:3 n-3 (9,12,15)].
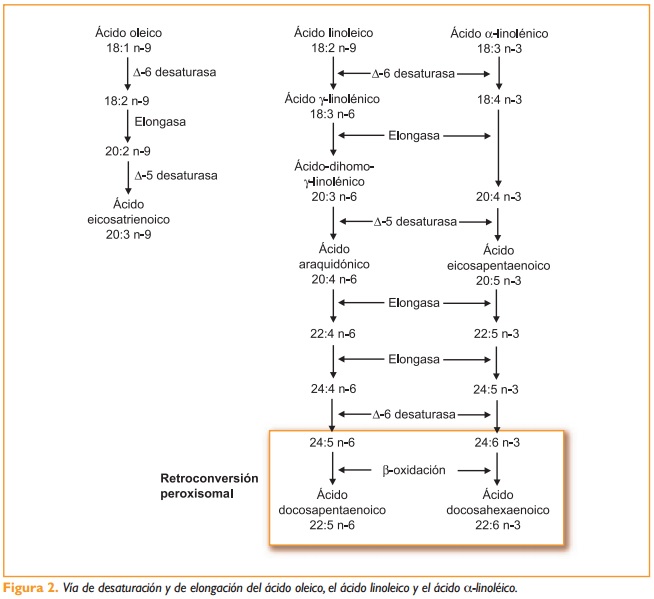
Dentro de los ácidos grasos poliinsaturados podemos encontrarnos con dos series o familias: por un lado, aquellos que presentan su primer enlace doble entre los carbonos seis y siete (empezando a contar desde el extremo metilo hasta el carboxilo esta vez), a los cuales llamamos serie o familia de los omega-6 (también ω-6 o n-6) y cuyo principal componente es el ácido linoleico antes mencionado; y por el otro lado, aquellos que presentan su primer doble enlace entre los carbonos tres y cuatro dentro de la estructura hidrocarbonada (ω-3 o n-3), siendo el ácido linolénico el máximo representante de esta familia, conocida como omega-3. Es a partir de estos dos compuestos desde donde tiene lugar la formación de sus derivados poliinsaturados de mayor longitud de cadena y número de insaturaciones. Los responsables de tal diferenciación son dos enzimas implicadas en dos procesos fundamentales en la conformación final de los ácidos grasos poliinsaturados de cadena larga y su enorme significado biológico: las elongasas, encargadas de aumentar el tamaño de la cadena hidrocarbonada mediante la adición de parejas de carbono; y las desaturasas, implicadas en la introducción de nuevas insaturaciones a la estructura. Conviene subrayar con trazo grueso que el ácido oleico, con una insaturación, no es un ácido graso esencial, ya que los mamíferos sí podemos formarlo a partir del ácido esteárico.
Dichas biotransformaciones tienen lugar en los microsomas del retículo endoplasmático, en una primera fase, y en los peroxisomas, en una fase final que conocemos como retroconversión peroximal, según la cual se produce la formación del ácido docosapentanoico a partir del C24:5 n-6 (serie omega-6) y el docosahexaenoico a partir del C24:6 n-3 (serie omega-3), de los que hablaremos a renglón seguido.
Con todo, es muy común el trato indiscriminado que podemos observar en medios de comunicación no especializados en cuanto a la atribución de según qué propiedades a los ácidos grasos omega 6 (generalmente proinflamatorias) respecto a los ácidos grasos omega 3 (antiinflamatorias), sin entrar en consideraciones sobre las muchas transformaciones intermedias que dichos ácidos grasos sufren, así como cuándo y por qué tienen lugar. Obviamente, reducir la bioquímica al juego de buenos y malos no hace sino aumentar aún más la confusión, más aún cuando unos y otros se necesitan y complementan. Algo a lo que ya nos tienen bastante acostumbrados con el clásico reduccionismo de colesterol malo (LDL) frente a colesterol bueno (HDL), cuando sabemos que tanto sin el uno como sin el otro nuestro organismo menguaría como un charco bajo el sol.
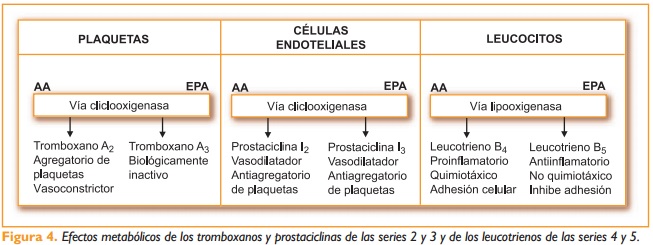
Estas propiedades de las que tanto nos hablan, no son fruto de los ácidos grasos poliinsaturados de cadena larga per se, sino de los productos que a partir de ellos se forman: los eicosanoides. Dichos eicosanoides son moléculas de veinte átomos de carbono que actúan como hormonas locales (paracrinas y autocrinas), modulando respuestas cardiovasculares, pulmonares, inmunitarias, reproductivas y secretoras. Entre ellos se encuentran las prostaglandinas (PG), tromboxanos (TX), leucotrienos (LT) y lipoxinas (LX), los cuales, a su vez, entran en lo que conocemos como la cascada de los eicosanoides para formar sus derivados metabólicos según accedan a la vía de la ciclooxigenasa (dando los derivados de prostaglandinas, prostaciclinas o tromboxanos) o la vía de la lipooxigenasa (leucotrienos).
Sabemos que cuando hablamos de ácidos grasos omega-6, partimos del ácido linoleico (C18:2 n-6), el cual puede darnos mediante las distintas elongaciones y desaturaciones diferentes ácidos grasos poliinsaturados de cadena larga: el ácido gamma-linolénico (C18:3 n-6); su derivado dihomogammalinolénico (C20:3 n-6); el eicosatrienoico (C20:3 n-9), también alcanzable en la serie del oleico; el muy a destacar ácido araquidónico (C20:4 n-6); y, finalmente, tras otros tantos puntos de elongación y desaturación, así como una fase de retroconversión, el ácido docosapentaenoico (C22:5 n-6)
Por su parte, partiendo del ácido linolénico (C18:3 n-3) de la serie omega-3, las diferentes biotransformaciones por las que éste puede pasar nos permite obtener los distintos ácidos grasos poliinsaturados de cadena larga: ácido eicosapentaenoico (C20:5 n-3) y ácido docosahexaenoico (22:6 n-3). Es importantísimo señalar que los beneficios del eicosapentaenoico sólo serán tales cuando dicho ácido graso sea consumido tal cual mediante la dieta; es decir, cuando su ingesta provenga de fuentes marinas o suplementos y no por las transformaciones del linolénico, por lo que no podemos tratar igualmente todos los ácidos grasos omega-3, ya que el ácido linolénico derivado, por ejemplo, de las semillas de lino o las nueces, tenderá a darnos el ácido docosahexaenoico y no el ácido eicosapentaenoico, obviando que cada uno de ellos producirá a su vez distintos derivados metabólicos de los eicosanoides, como veremos más adelante. Es por ello muy importante evitar toda homogeneización en el trato de la información que a menudo vemos en las publicaciones (especialmente internet: el peor divulgador científico de la historia), teniendo muy en consideración a partir de ahora que en lo que a la alimentación se refiere, los beneficios antiinflamatorios de la serie omega-3 única y exclusivamente vendrán de la mano del ácido eicosapentaenoico, ya que es éste y no el docosahexaenoico de los vegetales el que nos rendirá vía lipooxigenasa los leucotrienos de la serie 5 (LT5), los cuales poseen efectos antiinflamatorios e inhibitorios sobre la quimiotaxis y adhesión celular.
En cuanto a los distintos derivados de los eicosanoides según se formen estos a partir del ácido araquidónico (omega-6) o eicosapentaenoico (omega-3), mencionaremos a vuelapluma cuáles son éstos derivados y sus efectos fisiológicos.
El ácido araquidónico, el cual puede ingresar directamente a través de la dieta o ser producido a partir del linoleico, es incorporado a los fosfolípidos de las membranas celulares, siendo liberado por la acción de la fosfolipasa A2, y no por la lipoproteína lipasa cuando éste es transportado como VLDL desde el hígado, ya que ésta enzima sólo podría desgajarlo de las posiciones sn-1 y sn-3 de los triacilgliceroles y fosfolípidos, mientras que la fosfolipasa A2 sí actúa en la posición sn-2, donde se encuentra el ácido araquidónico. Una vez hidrolizado, el ácido araquidónico puede acceder tanto a la vía de la ciclooxigenasa como de la lipooxigenasa. En el primer caso, los productos derivados que pueden formarse son: tromboxanos de la serie 2 (TX2) en las plaquetas, teniendo acción vasoconstrictora y estimulante de la agregación plaquetaria; y prostaglandinas y prostaciclinas de la serie 2 (PGI2 y PCI2) en las células endoteliales, siendo inhibidores de la agregación plaquetaria y vasodilatadores. En el otro lado de la balanza, mediante la vía de la lipooxigenasa, los productos que se forman son los leucotrienos de la serie 4 (LT4) con efecto antagónico al de los LT5, por lo que poseen efecto proinflamatorio, quimiotáxico y estimulante de la adhesión celular.
En cuanto al ácido eicosapentaenoico, liberado del mismo modo que el araquidónico mediante la acción de la fosfolipasa A2, forma por vía de la ciclooxigenasa los tromboxanos de la serie 3 (TX3), un agregador más débil que el TX2; y las prostaglandinas y prostaciclinas de la serie 3 (PGI3 y PCI3), inhibidores de la agregación plaquetaria y vasodilatadores. Huelga aclarar que los derivados del eicosapentaenoico de la vía de la ciclooxigenasa poseen escasa actividad biológica, no ocurriendo lo mismo con su producto de la vía lipooxigenasa: los leucotrienos de la serie 5 (LT5). Y es que los leucotrienos de la serie 5 formados en los leucocitos tienen una potente acción antiinflamatoria, inhibitoria de la quimiotaxis y de la adhesión celular. Es por todo lo mencionado anteriormente por lo cual el ácido eicosapentaenoico tiene un potente efecto protector frente a la cardiopatía isquémica, hecho ampliamente estudiado sobre la población esquimal, en la cual el tiempo de sangría está incrementado respecto a la población normal. Por otro lado, considerando la responsabilidad de las prostaglandinas en los procesos de fiebre, dolor e inflamación, se sobreentiende cómo antiinflamatorios no esteroideos como el ibuprofeno pueden bloquear los mismos, al ser un inhibidor de la ciclooxigenasa. Del mismo modo, al estar implicados los tromboxanos en la constricción de los vasos sanguíneos y la agregación plaquetaria, cobran pleno sentido las evidencias científicas respecto a la relación existente entre dosis bajas de aspirina tomadas regularmente (del orden de 80 mg de aspirina infantil) y la reducción de probabilidad de ataque al corazón y embolias, al reducir la producción de tromboxanos. Por si fuera poco, sabemos además que la liberación de estos eicosanoides inflamatorios induce la producción de otros mediadores proinflamatorios mediante la activación del factor de transcripción nuclear kappa-B (NF-kappaB), dirigiéndose al núcleo celular y activando la síntesis de mediadores inflamatorios a través de la expresión génica de enzimas inflamatorias como las COX-2 y las citoquinas TNF-alfa y la interleucina-6 (señales implicadas en la comunicación celular). Siguiendo en el plano de la genética (en el que ahondaremos en otro momento) sabemos igualmente cómo estos ácidos grasos esenciales actúan como ligandos en lo que conocemos como receptores activados por proliferadores perxisomales (PPAR), una familia de receptores nucleares que media en la expresión génica de hormonas esteroideas, glucocorticoides, tiroxina, ácido retinoico y vitamina D. Sólo apostillar la enorme trascendencia que están alcanzando los PPAR en los últimos años, ya que son éstos receptores quienes se hallan implicados en según qué respuestas en función del ligando, de tal modo que sabemos de qué modo las grasas saturadas e isómeros trans, al presentar bajas cantidades de ácidos grasos esenciales, inducen la acumulación de ácidos grasos en los depósitos dada la disminución en la beta-oxidación ante la falta de estimulación de los PPAR-alfa, de igual que se modifica el perfil lipídico de las membranas celulares ante la baja disponibilidad de araquidónico, docosahexaenoico y eicosapentaenoico, estando todo ello relacionado con la resistencia a la insulina y la posterior diabetes de tipo 2, dislipidemia y obesidad.
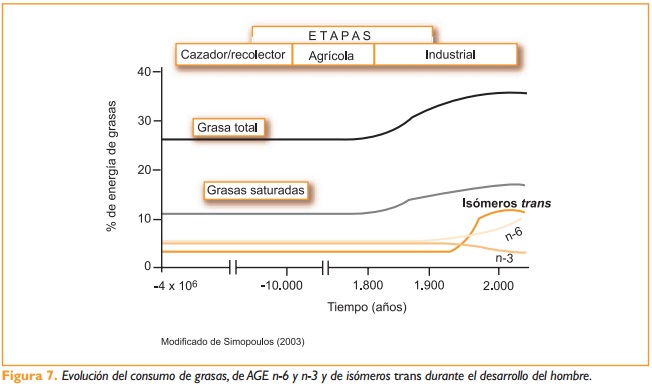
Así las cosas, vemos cómo los distintos eicosanoides tienen efectos antagónicos según provengan de un ácido graso u otro. Y es precisamente al arrimo de estos desequilibrios –pues equilibrio es el que debiera existir– de donde derivan multitud de enfermedades crónicas. De ahí la importancia de mantener un balance equilibrado entre los eicosanoides derivados del araquidónico y aquellos otros derivados del eicosapentaenoico. Con todo, ¿dónde cabría identificar dicho desbalance por el que prevalece la sobreproducción de los eicosanoides derivados del araquidónico en vistas a la enorme incidencia de cardiopatías? Pues en la propia alimentación. Precisamente es el actual modelo de alimentación occidental el que tiene la balanza volcada hacia la producción de proinflamatorios y vasoconstrictores en lugar de sus contrarios. Sabemos que la afinidad de la enzima delta-6-desaturasa (encargada de añadir insaturaciones) es mayor por el ácido linolénico (omega-3) que por el ácido linoleico (omega-6). Por lo tanto, altas cantidades de linolénico inhiben la producción de los derivados del linoleico (araquidónico principalmente), mientras que ingestas elevadas de linoleico inhiben la formación de los derivados del linolénico (especialmente docosahexaenoico, pues el eicosapentaenoico se alcanza mediante la dieta y no por biotransformaciones). Así las cosas, un 2% del aporte calórico total en forma de ácido linolénico (omega-3) bastaría para inhibir casi en su totalidad la transformación del linoleico (omega-6) en sus ácidos grasos derivados, mientras que se requeriría unas diez veces la cantidad de linoleico (omega-6) para inhibir la formación de los derivados del linolénico (omega-3). De ahí que el ratio óptimo entre omega-6/omega-3 deba estar alrededor del 5:1, produciéndose la inhibición equivalente entre el linoleico y linolénico con una relación de 14:1 (de la que no se obtendrían beneficios metabólicos). Con todo, el nudo gordiano del asunto de los omega-3 y omega-6 radica en lo que a lo estrictamente dietético se refiere. Y es que el ratio en occidente, lejos de acercarse a los 5:1 deseables, oscila entre el 16:1 y el 20:1, dependiendo de los países, siendo más acuciante en aquellos con una cultura culinaria en la que no tenga gran presencia los productos marinos, al contrario de lo que ocurre en muchas regiones orientales. Por si fuera poco, el aumento en el consumo de grasas hidrogenadas (p.ej. margarinas y productos de repostería) produce un aumento en lo que a los isómeros trans se refiere, claramente aterogénicos e implicados en la inhibición de la enzima delta-6-desaturasa y estructuralmente similares a las grasas saturadas, implicadas ambas en procesos de hipercolesterolemia y aterosclerosis. Con todo, no son pocas las empresas alimentarias (especialmente en el campo de las margarinas y leches) a las cuales no les duelen prendas a la hora de confundir alevosamente a los consumidores al añadir en los etiquetados el clásico ''enriquecido con omega-3'' para después presentar ratios de hasta 14:1 que, como hemos visto, promocionarían la vía de transformación de los omega-6 y no de los omega-3; es decir, la producción de eicosanoides derivados del araquidónico.
Según un estudio de Eroski Consumer, hasta un 26% de los productos analizados presentaron deficiencias notables en la composición nutricional de los mismos (leches enriquecidas, leches de soja, néctares y margarinas) de tal modo que lo que realmente añadían a sus productos no era más que ácido linolénico en forma de aceite de linaza, de soja u otras fuentes vegetales. El problema radica en que, como ya hemos hablado, el alfa linolénico no se puede convertir en eicosapentaenoico, por lo que los beneficios protectores del omega-3 en estos casos serían inexistentes. Por tanto, a la hora de buscar los beneficios del omega-3 (por eso comentamos que no se puede homogeneizar toda la familia omega) el producto deberá indicarnos de un modo explícito su adición de ácido eicosapentaenoico, algo que rara vez veremos, habida cuenta del incremento en los costes de producción que ello supondría. De ahí que la recomendación sea consumir eicosapentaenoico tal cual, a través de productos marinos. Tan es así que, para ilustrarlo numéricamente, 100 gramos de salmón presentan hasta 5.000 mg de eicosapentaenoico y docosahexaenoico, mientras que 100 gramos de margarina enriquecida aportaría unos 500 mg de los mismos (hablando de 100 gramos, cuando una tarrina completa contiene 250 gramos de margarina). Vemos así ese gran negocio abierto por según qué empresas a la hora de confundir con los productos enriquecidos y, por qué no, abusar de la confianza y desconocimiento de unos bienintencionados consumidores. Y es que, siguiendo con el caso del que hablamos, sabiendo que una cucharada grande de margarina son 15 gramos, un desayuno con margarina enriquecida con omega-3 nos rendiría…75 miligramos de eicosapentaenoico y docosahexaenoico, 66 veces menos que los 100 gramos de salmón. Todo ello sabiendo de la guerra abierta por la delta-6-desaturasa a la hora de pelear por los distintos ácidos grasos, y obviando que mínimamente el 0,5% de las calorías totales ingeridas debieran corresponderse con la familia de los omega-3 (siendo el eicosapentaenoico ingerido naturalmente) para así mejorar el perfil lipídico.
Para concluir, subrayar cómo debido a que los ácidos grasos omega-6 son muchísimo más abundantes que los omega-3, y cómo el perfil de éstos últimos que solemos encontrar en los alimentos no es el más adecuado, son muchas las investigaciones que se están llevando a cabo para optimizar la producción de eicosapentaenoico, como está ocurriendo en el campo de la microbiología, al encontrar bacterias en la microbiota de peces de agua salada con un alto contenido en este tipo de ácido graso poliinsaturado de cadena larga, utilizándose en cultivos para la obtención de aceites ricos en eicosapentaenoico y también docosahexaenoico. Un ácido graso –el docosahexaenoico– que también comienza a obtenerse de un modo incrementado mediante la carne de pollo y cerdo alimentados con aceites marinos, al igual que ocurre con los huevos de las gallinas. Vemos así cómo existe una auténtica demanda fruto del interés cada vez más exacerbado por mejorar el perfil lipídico de los individuos, toda vez que sabemos cómo estos desequilibrios son la palanca del desencadenamiento de muchísimas enfermedades crónicas. Con todo, mal que nos pese, las evidencias científicas actuales nos dicen muy a las claras que esta mejora pasa por el incremento en la ingesta natural de eicosapentaenoico. Claro que en la tan aireada dieta mediterránea no es precisamente este ácido graso el más promovido. Y ya se sabe: la ropa sucia hay que lavarla en casa.
 Fuente RSS
Fuente RSS

