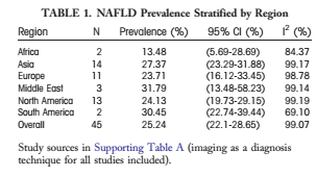
Hace tan sólo unos días veíamos publicada en The Lancet una minuciosa revisión sobre uno de los grandes problemas de la civilización actual y que tanto preocupa en el arriscado campo de la Salud Pública bajo la firma de Norbert S. et al. Hablamos del Hígado Graso No Alcohólico (NAFLD), una entidad clínica que avanza en nuestros días como si de una manada de bisontes americanos se tratara. Y es que la prevalencia del NAFLD crece ferozmente alrededor del mundo, de toda suerte que se estima que el 25% de la población se hallaría afectada por dicha enfermedad, mientras que en el caso de los niños hablaríamos del 3-10% en no obesos y un 34% en obesos en los países desarrollados. Un crecimiento que nos llega de la mano del mismo aumento en otras patologías no transmisibles como la diabetes tipo 2, enfermedad cardiovascular, obesidad, cáncer asociado a diabetes tipo 2 y enfermedades del hígado como cirrosis hepática y cáncer hepático. Todo un rosario de patologías sobre las que pesa sobremanera los estilos y hábitos de vida actuales, principalmente la dieta.
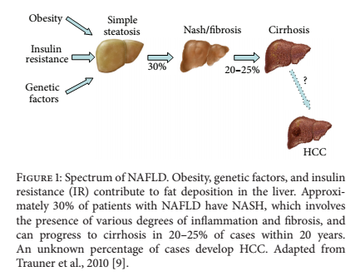
Así las cosas, el NAFLD podría ser categorizado histológicamente en hígado graso no alcohólico propiamente dicho, el cual se define como la presencia de al menos un 5% de esteatosis hepática sin evidencia de daño hepatocelular; mientras que el NASH o esteatohepatitis no alcohólica exigiría la presencia de al menos un 5% de esteatosis hepática e inflamación, con presencia de lesiones en los hepatocitos, con o sin fibrosis. Huelga señalar que la enfermedad cardiovascular es la principal causa de muerte en las personas con NAFLD, del mismo modo que estos sujetos con NAFLD tienen más probabilidades de desarrollar diabetes de tipo 2 y las personas con diabetes de tipo 2 ser más propensas a desarrollar NAFLD. De hecho, se estima que el 70% de las personas con diabetes de tipo 2 tiene NAFLD, trenzándose y retroalimentándose ambas patologías en una espiral que no acaba. Tan es así, que la propia diabetes representa un factor de riesgo para la progresión de NAFLD hacia NASH, cirrosis y mortalidad, motivo por el cual la esteatohepatitis no alcohólica o NASH está siendo considerada una nueva complicación de la diabetes de tipo 2, de modo que probablemente en un futuro no muy lejano sea rastreada del mismo modo en que se hace en relación a la nefropatía diabética y la retinopatía diabética. Un asunto desde luego nada baladí, habida cuenta del aumento en el riesgo de fibrosis hepática, carcinoma hepatocelular y mortalidad derivados del NASH. En cuanto al NAFLD como factor de riesgo independiente para la diabetes de tipo 2, existen trabajos al respecto que muestran cómo estos sujetos tendrían 5.5 veces más probabilidades de debutar en la enfermedad diabética. Del mismo modo, reseñar lo que varios autores señalan en cuanto a la relación entre la acumulación de grasa hepática y resistencia a la insulina, de tal suerte que cada una de ellas agravaría a la otra recíprocamente; es decir, ambas cabalgarían a toda brida por un complejo circuito bidireccional de cruces y puntos de encuentro, tal como revisan exhaustivamente los italianos Luca Valenti et al., del Instituto Nacional del Cáncer italiano en un trabajo para Liver International bajo el nombre de Nonalcoholic fatty liver disease: cause or consequence of type 2 diabetes?
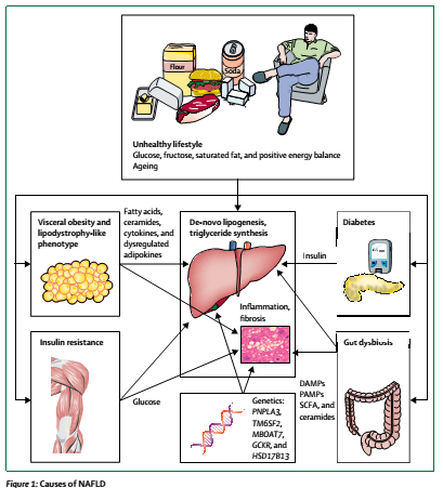
En lo que concierne a los estilos y hábitos de vida antes mencionados, sabemos que la sobrenutrición y el sedentarismo muy a menudo derivan en obesidad y esteatohepatitis, del mismo modo que un incremento en la ingesta de glucosa y fructosa puede inducir una lipogénesis hepática de novo concomitante, inflamación subclínica en el tejido adiposo, así como resistencia a la insulina en tejido adiposo, hígado y músculo esquelético. Por otro lado, hallaríamos igualmente un incremento en la liberación de citoquinas proinflamatorias y una desregulación en la secreción de adipoquinas desde el tejido adiposo capaces de contribuir al proceso de almacenamiento de lípidos en el hígado. Otros elementos contribuidores en el desarrollo de NAFLD serían las ceramidas y productos derivados de una disbiosis intestinal inducida por unos hábitos dietéticos pobres, tales como los lipopolisacáridos (LPS) o endotoxinas de las bacterias gram negativas que pueblan ese submundo de pasillos subterráneos que es nuestro colon. De hecho, un aumento en la permeabilidad intestinal en presencia de disbiosis podría permitir la inflamación del tejido adiposo, esteatosis hepática e inflamación hepática. Cabe también darle su espacio e importancia al propio envejecimiento y determinados cambios tanto hereditarios como adquiridos de naturaleza genética y epigenética, los cuales tendrían su propio efecto acumulativo en el propio fenotipo de envejecimiento desarrollado por el sujeto. Así pues, el declinar en la masa muscular y el deterioro funcional asociado al envejecimiento influiría en el devenir de muchas de las enfermedades crónicas no transmisibles como el NAFLD. Sabemos que la disminución en los niveles de hormonas sexuales y expresión de receptores para éstas tanto en hombres como en mujeres no solo resulta en una redistribución del tejido adiposo desde la parte inferior del cuerpo hacia la parte superior y desde los depósitos adiposos subcutáneos hacia los viscerales, sino que además supone un incremento del almacenamiento ectópico de lípidos en el hígado
Volviendo a la relación entre patrones dietéticos y NAFLD, sabemos que la misma malnutrición por exceso que juega un rol tan importante en el desarrollo de la obesidad y otras comorbilidades asociadas es la que también cumple idéntico papel en la aparición del NAFLD como factor de riesgo asociado. Tan es así, que la ganancia por sí misma de 3-5 kg puede predecir el desarrollo del NAFLD, al margen del IMC de base. Pero no hablaríamos tanto del cuánto comemos sino del qué y el cuándo. Sabemos que los niños americanos consumen el 25% de sus calorías como snacks; es decir, fuera de las comidas principales del día. Al respecto, un ensayo clínico publicado en 2014 en Hepatology estudió el asunto, de modo que 36 adultos sanos fueron aleatorizados en un grupo con un patrón de consumo hipercalórico en un 40% por 6 semanas u otro eucalórico de control a fin de medir su influencia en los niveles de triglicéridos intrahepáticos. El grupo de sobreconsumo calórico ingirió el exceso bien mediante ingestas mayores de grasas + azúcar o solamente azúcar, consumidos con o entre las tres comidas principales del día, de toda suerte que dicho sobreconsumo viniera dado por un aumento en el tamaño de las comidas o bien por un aumento en el número de las mismas. Los patrones hipercalóricos dieron un aumento en el IMC, pero fue el incremento en el número de comidas el que produjo un mayor aumento en la infiltración de grasa intrahepática (46% en el grupo grasas + azúcares vs 110% grupo azúcar), algo que no se observó en el grupo de aumento de las raciones. Con estos mimbres, los autores del trabajo, investigadores del Departamento de Endocrinología y Metabolismo del Centro Académico de Medicina de Ámsterdam, sugirieron en sus conclusiones finales que el fenómeno de ‘snacking’, tan común en el contexto de la dieta occidental, sería un contribuidor independiente de la esteatosis hepática y la obesidad.
Por otro lado, existe evidencia al respecto de cómo una reducción en el consumo de alimentos procesados y ricos en fructosa producen un descenso en los productos de glucosilación avanzada (AGEs), los cuales se hallan relacionados con la propia etiología de la diabetes y otras alteraciones metabólicas. Sabemos que estos productos de glucosilación avanzada se hallan elevados en pacientes con esteatohepatitis no alcohólica o NASH, en comparación con los sujetos con esteatosis simple y los controles sanos, hallándose asimismo correlacionado positivamente con el fenómeno de resistencia a la insulina y negativamente con los niveles de adiponectina. Hacer notar que los refrescos de cola, con su colorante caramelo, son ricos en estas glicotoxinas, las cuales según ciertos trabajos aumentarían la resistencia a la insulina, inflamación, al tiempo que exacerbarían la lesión hepática, esteatohepatitis y fibrosis hepática. Claro que si hay una mano negra tras estos niveles elevados de AGEs, ésta sería el elevado consumo de azúcares añadidos en la dieta occidental, muchas de las veces ocultos.
De este modo, existe suficiente evidencia respecto a la asociación entre consumo de azúcar y NAFLD, considerando a estos azúcares añadidos los hallados como sacarosa o fructosa, entre otros, a las bebidas azucaradas o refrescos, zumos de frutas industriales y otras bebidas, así como a ciertos alimentos que ya conocemos sobradamente, p.ej. todo lo encontrado en los stands de desayunos y meriendas de nuestros supermercados. Sabemos que un patrón dietético con un elevado consumo de fructosa y glucosa produce un aumento en los niveles de síntesis intrahepática de triglicéridos. En lo que a la fructosa se refiere, su consumo elevado se asocia con alteraciones en la microbiota intestinal, aumentando la permeabilidad intestinal, favoreciendo el fenómeno de endotoxemia, producción de TNF o Factor de Necrosis Tumoral a nivel hepático, peroxidación lipídica y esteatosis. Además, la fructosa promueve la producción de ácido úrico, el cual causa estrés oxidativo y resistencia a la insulina. Una ingesta elevada que vendría de la mano de un consumo alto de bebidas o refrescos azucarados, los cuales se hallarían asociados a una mayor infiltración de grasa intrahepática. Un análisis del famoso Estudio de Framingham observó una asociación directa dosis-respuesta entre el consumo de refrescos e hígado graso, con un aumento del riesgo de NAFLD del 61% en consumidores de bebidas azucaradas frente a los no consumidores.
En 2012, un equipo de Dinamarca liderado por María Maerks estudió 47 sujetos obesos, los cuales fueron asignados aleatoriamente a cuatro grupos diferentes durante seis meses con diferentes patrones de ingesta: uno de ellos ingirió un litro diario de Coca Cola normal; otro, un litro de leche desnatada; el tercer grupo, un litro de Coca Cola diet; y un último grupo, un litro de agua. En relación a los otros tres grupos, los individuos del grupo de Coca Cola mostraron un aumento relativo desde el inicio hasta los seis meses de la intervención de un 132-143% más en los niveles de grasa hepática; 117-221% en la grasa muscular; 24-31% en la visceral; y un 32% en los triglicéridos totales. Reseñar que, pese a lo aparentemente superlativo de la ingesta diaria de un litro de Coca Cola, considerar que la ingesta de la misma en los Estados Unidos en jóvenes de 12-29 años es del orden de 1.8 L diarios y 0.5 L entre los individuos de todas las edades, por lo que dicha ingesta refleja un patrón de consumo occidental totalmente factible. Claro que existirían otros determinantes y ayudas terapéuticas en relación al patrón dietético.
Hace un mes, un estudio de M Drummen et al., del Departamento de Nutrición y Ciencias del Movimiento de la Universidad Médica de Maastricht, siguió a 25 individuos obesos durante dos años, los cuales llevaron a cabo una primera fase de pérdida de peso (8% del peso inicial) y una fase posterior de mantenimiento, en la cual tuvieron una ingesta más elevada de proteínas que acabó por producir una reducción en los niveles de grasa hepática y visceral. Una grasa hepática que se halló relacionada positivamente con un aumento en el índice HOMA-IR de resistencia a la insulina e inversamente relacionada con el Índice de Matsuda de Sensibilidad a la Insulina (ISI), independientemente del IMC. Unas observaciones acordes a lo ya visto tanto en individuos sanos como obesos y diabéticos de tipo 2, según las cuales la suplementación proteica induciría una reducción concomitante en los niveles de grasa intrahepática. Tan es así, que en el trabajo de Drummen et al., el número de participantes con NAFLD pasó de 15 a 7 después de los dos años de intervención. Los elementos fisiológicos involucrados en esta interrelación entre grasa hepática y resistencia a la insulina serían una merma en las vías de señalización de la insulina fruto de la acumulación de grasa intrahepática y el efecto inhibitorio de la insulina sobre la gluconeogénesis, estimulando la síntesis de glucógeno. Además, la resistencia a la insulina en el tejido adiposo incrementaría la lipolisis, aumentando la circulación de ácidos grasos no esterificados tomados por el hígado. La estrecha relación entre grasa hepática e hiperinsulinemia además vendría dada por una reducción en el aclaramiento hepático de la insulina. Nos hallaríamos así sumidos en un círculo vicioso al arrimo del cual la alta concentración de lípidos intrahepáticos inhibiría la propia acción de la insulina en el hígado, propiciando un aumento en el nivel portal de insulina e incremento intrahepático de lípidos. Un nudo gordiano que podría verse desgajado por la propia actividad física, de tal manera que ésta induciría una mejora en el control de la glucosa y oxidación de lípidos a través del aumento en la expresión de los transportadores de glucosa GLUT-4 en el músculo estriado, expresión y actividad de la enzima glucógeno sintasa, receptores de insulina y almacenamiento de glucógeno en hígado y músculo esquelético.
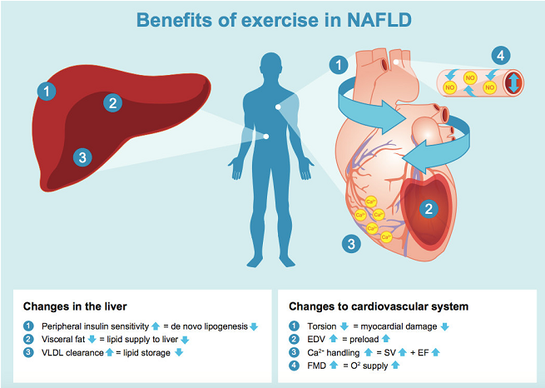
En lo que se refiere al estilo de vida sedentario, cada vez tenemos más pruebas y evidencia científica al respecto de cómo este estilo pausado y sedentario puede facilitar el desarrollo del NAFLD. De hecho, un trabajo de 2016 publicado en el British Medical Journal halló una asociación positiva entre el tiempo sentado (>7.1 horas al día) y una mayor prevalencia de NAFLD. No obstante, ateniéndonos a la actividad física como instrumento de prevención y tratamiento en el NAFLD, sabemos que tanto el ejercicio aeróbico como el de fuerza logra notables mejoras en la reducción del volumen de infiltración de grasa hepática, independientemente de la pérdida de peso corporal. La primera evidencia de que la práctica regular de ejercicio aeróbico reducía per se la cantidad de lípidos hepáticos en sujetos obesos vino de la mano de un trabajo de intervención durante cuatro semanas en el que los sujetos obesos y sedentarios sometidos a un protocolo de entrenamiento aeróbico tuvieron reducciones significativas de grasa visceral, triglicéridos hepáticos y ácidos grasos libres, aun sin cambios significativos en la pérdida de peso. Unos resultados también observados cuando de ejercicio de fuerza hablamos. Hallsworth et al. demostraron que el ejercicio de fuerza tres veces por semana durante ocho semanas fue efectivo en la reducción de lípidos intrahepáticos en sujetos con NAFLD. Tres años después, en 2015, el mismo autor publicaba un nuevo trabajo en relación al NAFLD y el ejercicio físico, en este caso mediante ejercicio interválico de alta intensidad con cicloergómetro 3 veces por semana durante 12 semanas. Los sujetos del grupo de cicloergómetro lograron una reducción en la infiltración de triglicéridos intrahepáticos del 27%, con una pérdida de masa grasa corporal de 1.8 kg, además de mejoras en la función diastólica y reducción en los niveles de transaminasas. Otro trabajo realizado en Italia en 2013 comparó el ejercicio aeróbico y el ejercicio de fuerza en sujetos diabéticos con NAFLD durante 16 semanas. El ejercicio aeróbico consistió en 60 minutos, 3 días a la semana con actividad a intensidad moderada-vigorosa, mientras que el grupo de fuerza trabajó 60 minutos, 3 días a la semana realizando 3 series de 10 repeticiones al 70-80% del VO2 max. Al finalizar el estudio, los investigadores concluyeron que el ejercicio de fuerza fue tan efectivo como el clásico aeróbico en la reducción de la infiltración de grasa intrahepática (32% aeróbico vs 25.9% fuerza), con mejoras en la hemoglobina glicosilada, HDL, triglicéridos y sensibilidad a la insulina. Un tipo de actividad física –fuerza– que cumple además con el añadido de mejorar los niveles de masa muscular, fuerza y sensibilidad a la insulina en este grupo, junto con una mayor adherencia tanto en jóvenes como en adultos maduros. Del mismo modo, sabemos que el ejercicio de fuerza parece tener un efecto beneficioso en NAFLD mejorando los niveles circulantes de ácidos grasos libres y captación de glucosa, reduciendo así el impacto de la lipogénesis de novo mediada por la insulina. Debemos tener en cuenta que en individuos sanos normoglucémicos, la lipogénesis hepática de novo contribuye aproximadamente en un 5% en ayunas y 18-23% en el estado postprandial a los niveles de lípidos intrahepáticos, mientras que esta lipogénesis de novo se hallaría incrementada de un modo constante en el NAFLD, contribuyendo aproximadamente en un 26% a la mencionada infiltración de grasa intrahepática, independientemente del estado de alimentación. Otra de las vías por las cuales la actividad física sería beneficiosa en el tratamiento del NAFLD sería la propia atenuación del estado inflamatorio, en gran parte gracias al efecto endocrino y paracrino de las mioquinas (citoquinas y otros péptidos producidos y liberados por las fibras musculares) en respuesta a la contracción muscular.
A la hora de determinar qué actividad física realizar y a qué intensidad y duración, podríamos reseñar los tres puntos descritos en un trabajo de 2016 publicado en el Journal of Diabetes Research por Claudia P. Oliveira et al.: 1) 20-60 minutos o más de ejercicio aeróbico a intensidad moderada (45-70% del VO2 max) al menos cinco días a la semana e implicando grandes grupos musculares. 2) Ejercicio de fuerza a intensidad moderada-alta tres veces por semana. 3) A fin de lograr beneficios indirectos asociados a la pérdida de peso, realizar más de 250 minutos de actividad física a la semana. No obstante, hemos de ser conscientes que este cumplimiento en sujetos con NAFLD puede ser menor al previsto habida cuenta que existen pruebas de que en ellos la fatiga se halla acentuada con la realización del ejercicio, hallándose además asociada a mayor inactividad y somnolencia diurna, por lo que es de vital importancia incorporar un patrón de actividad física que genere mayor adherencia y requiera una menor demanda de tiempo y esfuerzo para idénticos resultados, algo que cumple sobradamente el ejercicio de fuerza. Una fatiga, por cierto, similar a la observada en pacientes con cirrosis biliar primaria y la cual se hallaría ligada a una menor funcionalidad física. Por todo ello, la elección del tipo de ejercicio físico deberá estar basada en las preferencias y capacidades del paciente a fin de ser mantenidas a largo plazo. Y siempre considerando el beneficio añadido que nos brindará en cuanto a la reducción de peso corporal, pese a que esta actividad física reduzca los niveles de grasa intrahepática per se.
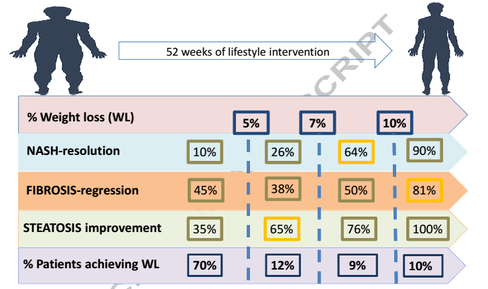
Recalcar asimismo que pérdidas de peso del 4-14% logran reducciones en los niveles de infiltración de triglicéridos intrahepáticos del 35-81%. La importancia de la pérdida de peso se destaca en personas con NASH, donde la pérdida de peso >7% se asocia con una regresión clínicamente significativa de la enfermedad. No obstante, hemos de ser conscientes de que los sujetos con NAFLD tienen una menor preparación y motivación para la adopción en los cambios de hábitos de vida, dos elementos mollares en lo que a adherencia se refiere en el fenómeno de pérdida ponderal, teniendo en cuenta la dificultad existente a la hora de mantener en el largo plazo la pérdida de peso lograda en el corto y medio plazo, tal y como recoge abundante literatura al respecto. Ha sido repetidamente demostrado que la pérdida de peso lograda con la dieta es más alta a los 6 meses de seguimiento y, posteriormente, se produce una paulatina recuperación de peso que hace que se logre solamente de 3 a 4 kg de reducción de peso a los 2 años de seguimiento. Sin embargo, incluso existiendo recuperación de peso después de la intervención dietética, permanecería el efecto beneficioso a largo plazo sobre la grasa del hígado y la resistencia a la insulina, quizás porque la propia intervención lograra ciertos cambios en el estilo de vida sostenibles en el tiempo. Por su parte, en el trabajo de Vilar-Gómez et al., sólo el 10% de los pacientes (29/293) logró una pérdida de peso del 10%, mientras más del 70% de la cohorte (208/293) no consiguió perder el 5% de su peso corporal. En los pacientes con resolución en la esteatohepatitis no alcohólica o NASH, el determinante más clave fue mantener al paciente lejos de la recuperación del peso, como a bien tiene reseñar el catedrático de la Universidad de Sevilla Romero-Gómez en Journal of Hepatology con una brillante revisión: Treatment of NAFLD with diet, physical activity and exercise. En el mismo, pone el foco sobre uno de las conclusiones del controvertido Look AHEAD, un trabajo prospectivo sobre el que siguieron a 5145 individuos obesos con diabetes de tipo 2 durante 9.6 años y en el que la intervención en los hábitos de vida a largo plazo produjo una pérdida de peso igual o mayor al 5% en el 50% de los participantes.
En cuanto al diagnóstico del NAFLD, sabemos que de poco o nada sirve el estudio de las enzimas hepáticas. Existe literatura al respecto de cómo concentraciones plasmáticas de hasta dos veces el límite superior del rango normal de alanina aminotransferasa o ALT (>70 U/L) predice la esteatohepatitis no alcohólica con una sensibilidad del 50% y una especificidad del 61%, tal y como se sustrae del trabajo de Younossi ZM et al. publicado en 2017 en Hepatology, el mismo autor que en 2016 reportó en un metaanálisis global una prevalencia de NASH del 59% en pacientes con NAFLD. Es por ello que, dado que la mayoría de sujetos con NAFLD muestran niveles normales de aminotransferasas hepáticas, podamos hablar de una patología altamente subdiagnosticada. Por otro lado, considerando que la fase de fibrosis en la que se halle el sujeto es el mayor determinante de muerte por enfermedad hepática y cardiovascular en NAFLD, se hace necesaria la creación de escalas de puntuación no invasivas basadas en parámetros clínicos como edad, IMC, recuento plaquetario, transaminasas, glucosa en ayunas alterada o diabetes. Entre las escalas de puntaje, el NAFLD fibrosis score (NFS) y el fibrosis-4 (FIB-4) index tienen una mayor sensibilidad y especificidad para el diagnóstico de fibrosis avanzada (fibrosis en fase F3-F4) con un valor predictivo positivo del 80% y un valor predictivo negativo del 90%.
Así las cosas, la sociedad actual se topa con otro molesto chino en el zapato que nos persigue, se nos adhiere y, en definitiva, se suma al carro de las enfermedades no transmisibles que asedian a las sociedades occidentales. Unas patologías que crecen como los hongos después de la lluvia al arrimo y al abrigo de unos hábitos de vida mal adquiridos y fácilmente revertibles, como lo son el sedentarismo y los patrones de consumo alimentario modernos. O, tal y como señala Romero en el trabajo referenciado, lo que viene a ser el fenotipo del triple hit conductual: sedentarismo, baja actividad física y dieta pobre. El mismo que propone poner los pies contra la pared desde el ámbito clínico a la hora de advertir a los pacientes sobre los riesgos del NAFLD mediante el modelo de las 5As: ask, advise, asesses, assist and arrange. Y es que sólo desde una perspectiva de corresponsabilidad clínicos-pacientes y el ahondamiento en el empoderamiento de estos últimos podrá progresarse en un terreno que comienza a convertirse en un auténtico pantanal fangoso. Todo lo demás no será sino ahuyentar tábanos a sombrerazos.
REFERENCIAS:
-Valenti, L et al. Nonalcoholic fatty liver disease: cause or consequence of type 2 diabetes? Liver International, 36(11), 1563–1579.
-N. A. Johnson et al. Aerobic exercise training reduces hepatic and visceral lipids in obese individuals without weight loss,” Hepatology, vol. 50, no. 4, pp.1105–1112, 2009.
-Thoma C, Day CP, Trenell MI. Lifestyle interventions for the treatment of non-alcoholic fatty liver disease in adults: a systematic review. J Hepatol 2012; 56: 255-266
-Hallsworth K et al. Modified high-intensity interval training reduces liver fat and improves cardiac function in non-alcoholic fatty liver disease: a randomized controlled trial. Clin Sci (Lond) 2015;129: 1097-1105
-Hallsworth K et al. Resistance exercise reduces liver fat and its mediators in non-alcoholic fatty liver disease independent of weight loss. Gut 2011; 60: 1278-1283
-Bacchi E et al. Both resistance training and aerobic training reduce hepatic fat content in type 2 diabetic subjects with nonalcoholic fatty liver disease (the RAED2 Randomized Trial). Hepatology 2013; 58: 1287-1295
-Oliveira CP. et al. Nutrition and Physical Activity in Nonalcoholic Fatty Liver Disease. J Diabetes Res. 2016;2016:4597246.
-Haufe S et al. Longlasting improvements in liver fat and metabolism despite body weight regain after dietary weight loss. Diabetes Care 2013;36:3786-3792
-Romero-Gómez et al. Treatment of NAFLD with diet, physical activity and exercise. J Hepatol. 2017 Oct;67(4):829-846
-Koopman KE. et al, Hypercaloric diets with increased meal frequency, but not meal size, increase intrahepatic triglycerides: a randomized controlled trial. Hepatology. 2014 Aug;60(2):545-53.
-Golabi P. et al. Effectiveness of exercise in hepatic fat mobilization in nonalcoholic fatty liver disease: Systematic review. World J Gastroenterol 2016 July 21; 22(27): 6318-6327
-Zelber-Zagi S. et al. Nutrition and physical activity in NAFLD: An overview of the epidemiological evidence. World J Gastroenterol 2011 August 7; 17(29): 3377-3389
-JL Newton et al. Fatigue in non-alcoholic fatty liver disease (NAFLD) is significant and associates with inactivity and excessive daytime sleepiness but not with liver disease severity or insulin resistance. Gut 2008;57:807–813
-Mathijs Drummen et al. Long-term effects of increased protein intake after weight loss on intrahepatic lipid content and implications for insulin sensitivity - a PREVIEW study. Am J Physiol Endocrinol Metab. 2018 Aug 7.
-M Maersk et al. Sucrose-sweetened beverages increase fat storage in the liver, muscle, and visceral fat depot: a 6-mo randomized intervention study. Am J Clin Nutr 2012;95:283–9.
-Norbert S. et al. Non-alcoholic fatty liver disease: causes, diagnosis, cardiometabolic consequences, and treatment strategies. Lancet Diabetes Endocrinol 2018
-Younossi ZM. et al. Global Epidemiology of Nonalcoholic Fatty Liver Disease—Meta-Analytic Assessment of Prevalence, Incidence, and Outcomes. Hepatology. 2016 Jul;64(1):73-84
-Valenti, L et al. Nonalcoholic fatty liver disease: cause or consequence of type 2 diabetes? Liver International, 36(11), 1563–1579.
-N. A. Johnson et al. Aerobic exercise training reduces hepatic and visceral lipids in obese individuals without weight loss,” Hepatology, vol. 50, no. 4, pp.1105–1112, 2009.
-Thoma C, Day CP, Trenell MI. Lifestyle interventions for the treatment of non-alcoholic fatty liver disease in adults: a systematic review. J Hepatol 2012; 56: 255-266
-Hallsworth K et al. Modified high-intensity interval training reduces liver fat and improves cardiac function in non-alcoholic fatty liver disease: a randomized controlled trial. Clin Sci (Lond) 2015;129: 1097-1105
-Hallsworth K et al. Resistance exercise reduces liver fat and its mediators in non-alcoholic fatty liver disease independent of weight loss. Gut 2011; 60: 1278-1283
-Bacchi E et al. Both resistance training and aerobic training reduce hepatic fat content in type 2 diabetic subjects with nonalcoholic fatty liver disease (the RAED2 Randomized Trial). Hepatology 2013; 58: 1287-1295
-Oliveira CP. et al. Nutrition and Physical Activity in Nonalcoholic Fatty Liver Disease. J Diabetes Res. 2016;2016:4597246.
-Haufe S et al. Longlasting improvements in liver fat and metabolism despite body weight regain after dietary weight loss. Diabetes Care 2013;36:3786-3792
-Romero-Gómez et al. Treatment of NAFLD with diet, physical activity and exercise. J Hepatol. 2017 Oct;67(4):829-846
-Koopman KE. et al, Hypercaloric diets with increased meal frequency, but not meal size, increase intrahepatic triglycerides: a randomized controlled trial. Hepatology. 2014 Aug;60(2):545-53.
-Golabi P. et al. Effectiveness of exercise in hepatic fat mobilization in nonalcoholic fatty liver disease: Systematic review. World J Gastroenterol 2016 July 21; 22(27): 6318-6327
-Zelber-Zagi S. et al. Nutrition and physical activity in NAFLD: An overview of the epidemiological evidence. World J Gastroenterol 2011 August 7; 17(29): 3377-3389
-JL Newton et al. Fatigue in non-alcoholic fatty liver disease (NAFLD) is significant and associates with inactivity and excessive daytime sleepiness but not with liver disease severity or insulin resistance. Gut 2008;57:807–813
-Mathijs Drummen et al. Long-term effects of increased protein intake after weight loss on intrahepatic lipid content and implications for insulin sensitivity - a PREVIEW study. Am J Physiol Endocrinol Metab. 2018 Aug 7.
-M Maersk et al. Sucrose-sweetened beverages increase fat storage in the liver, muscle, and visceral fat depot: a 6-mo randomized intervention study. Am J Clin Nutr 2012;95:283–9.
-Norbert S. et al. Non-alcoholic fatty liver disease: causes, diagnosis, cardiometabolic consequences, and treatment strategies. Lancet Diabetes Endocrinol 2018
-Younossi ZM. et al. Global Epidemiology of Nonalcoholic Fatty Liver Disease—Meta-Analytic Assessment of Prevalence, Incidence, and Outcomes. Hepatology. 2016 Jul;64(1):73-84

 Fuente RSS
Fuente RSS

