«A la vejez, poco dormir y mucho gruñir», reza socarronamente el dicho popular a fin de ilustrar la que es una realidad manifiesta en la tercera edad. A saber, la falta de sueño. Sin embargo, en esta vida moderna tan nuestra, cada vez es más común dicha deprivación del sueño entre jóvenes y adultos de media edad, ya sea por hábitos y costumbres de ocio como por horarios y turnos de trabajo nocturnos, además de otras muchas más causas ligadas al entretenimiento tecnológico. Claro que estos cambios y desórdenes en el puzle del sueño tienen implicaciones clínicas mucho más complejas y de calado que la simple pachorra mañanera fruto de la falta de horas de descanso. Una de ellas sería la estrecha relación entre la restricción del sueño y el aumento en la adiposidad y pérdida de masa magra. Y no sólo eso, sino que hablaríamos también de una resistencia incrementada a la pérdida de ese tejido adiposo aumentado.
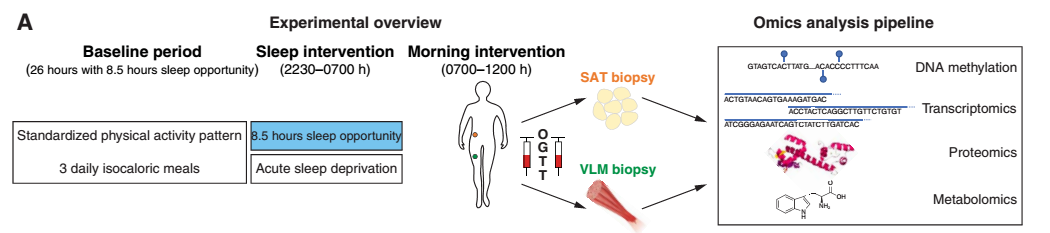
En agosto de este mismo año, veía la luz un interesante trabajo publicado en Science Advances rubricado por diversos investigadores de distintos países, desde Suecia a Alemania, pasando por China, bajo el liderazgo de Jonathan Cedernaes, del Departamento de Neurociencia de la Universidad de Uppsala, Suecia. En el mismo, 15 individuos sanos fueron monitoreados durante dos noches completas (desde las 22.30 hasta las 07.00), una de las veces manteniéndolos despiertos durante toda la noche y otra permitiéndoles dormir. La mañana después de cada intervención, los investigadores tomaron biopsias del tejido adiposo subcutáneo y músculo esquelético de los participantes, así como muestras de sangre. El objetivo de las mismas fue el de hallar cambios en la metilación del ADN, una de nuestras huellas epigenéticas más valiosas. Reseñar que cuando hablamos de epigenética, hacemos referencia al estudio de los elementos que regulan la expresión de nuestros genes sin alterar la secuencia de ADN; es decir, sin desbaratar el rosario de nucleótidos. Sería, por tanto, la chapa y pintura de nuestro ADN y, como tal, gozaría de un carácter reversible y modificable. Decir asimismo que dicho epigenoma se vería influenciado fundamentalmente por factores ambientales como la dieta, el estrés o, en este caso, el sueño.
En el caso que nos ocupa, se pudo observar que la restricción de sueño aguda produjo un patrón específico de metilaciones en los genes reloj encargados de regular nuestro ritmo circadiano, así como cambios en el grado de metilación del ADN en genes relacionados con tejidos específicos como el adiposo y el músculo esquelético. Una huella genética que reflejaría un aumento en la capacidad para almacenar grasa durante la deprivación del sueño y un aumento en el catabolismo muscular nocturno, el cual alteraría por sí mismo la homeostasis de la glucosa y motivo por el cual los participantes evidenciaron una pérdida en la sensibilidad a la glucosa tras la restricción del sueño.
Así las cosas, la restricción aguda –como sería un turno de noche en el trabajo– implicaría un cambio en la utilización de los distintos sustratos energéticos capaz de aumentar la oxidación no glucolítica e incrementando el catabolismo proteico del tejido muscular, favoreciendo así la hiperglucemia. Existiría, por tanto, una regulación negativa de las vías glucolíticas en el tejido esquelético, mientras que esta misma vía se hallaría sobre regulada en el tejido adiposo subcutáneo. Ello implicaría hipotéticamente que la restricción de sueño aguda podría inducir ciertas reprogramaciones vía metilación del ADN en nuestro tejido adiposo que facilitara un aumento en la adiposidad misma. De igual, los niveles de proteínas estructurales del músculo esquelético disminuirían en respuesta a esta misma reducción de sueño, en contraste con un aumento en las proteínas relacionadas con la adipogénesis en el tejido adiposo. Estos dos fenómenos explicarían por sí mismos gran parte o la totalidad de los fenotipos asociados a la restricción de sueño. A saber, ganancia de adiposidad y pérdida de masa magra.
Así pues, dichos cambios epigenéticos socavarían la llamada memoria metabólica. Un patrón de metilaciones que han sido observados en otros trabajos con individuos obesos y con diabetes de tipo 2, por lo que hablaríamos de disrupciones metabólicas compartidas. Con todo, el presente trabajo no hace sino ahondar en algo que ya viene siendo un foco de investigación desde hace algunos años. Sabemos por trabajos tanto con humanos como con animales que la pérdida de sueño promueve una pérdida de masa muscular concomitante. En roedores, la deprivación de sueño posee un efecto catabólico que se asemeja a la malnutrición proteica. Por su parte, estudios metabolómicos han mostrado que la pérdida de sueño promueve un estado manifiesto de catabolismo en sangre y orina, de igual que trabajos de cohorte con adultos de mediana edad y ancianos han observado una asociación entre pocas horas de sueño y menor masa muscular. No en vano, 1-2 noches de deprivación del sueño lleva consigo una excreción de nitrógeno urinario durante 24 horas aumentada, lo que denota un catabolismo proteico endógeno.
Una de las razones de estos cambios a nivel de composición corporal tendría que ver con diferentes patrones neuroendocrinos asociados a la restricción de sueño. Así, se ha podido observar que pérdidas de sueño agudas aumentan los niveles de cortisol, una hormona eminentemente catabólica. Para añadir pólvora al fuego, sabemos que esta restricción de sueño produce asimismo una reducción en los niveles de testosterona, al tiempo que se abole la liberación de hormona de crecimiento durante la noche, la cual tendría lugar en la tercera fase del sueño sin movimientos oculares rápidos (NMOR) o sueño de ondas lentas.
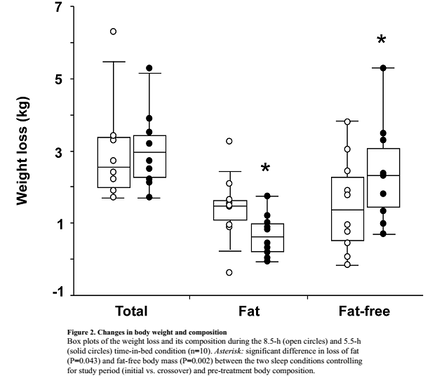
Con todo, esta desincronización circadiana a través de la restricción del sueño tendría importantes connotaciones no sólo a nivel de composición corporal, sino también en cuanto al uso de los distintos sustratos energéticos. En 2010, Nedeltcheva et al., de la Universidad de Chicago, llevó a cabo el primer trabajo a fondo sobre el asunto, realizando un ensayo en el que 10 individuos con sobrepeso fueron sometidos durante 14 días a una restricción calórica en condiciones controladas con una oportunidad de sueño de 5.5 o 8.5 horas, según el grupo de intervención. Aquellos que durmieron 5.5 horas o menos perdieron un 55% menos de grasa que aquellos que durmieron hasta 8.5 horas (0.6 kg vs 1.4 kg), al tiempo que aumentaron la pérdida de masa muscular en un 60% (2.4 kg vs 1.5 kg). Asimismo, el déficit de energía durante las 5.5 horas de descanso en la cama fue de 550 kcal/d, en comparación con los 920 kcal/d durante las 8.5 horas de descanso.
Por tanto, conocemos que la falta de sueño puede modificar las respuestas neuroendocrinas asociadas a la ingesta de alimentos y sus efectos metabólicos derivados. En el trabajo de Nedeltcheva, aquellos que dormían menos horas tenían más hambre, mayor circulación de grelina –hormona orexigénica– y menores niveles de leptina –hormona anorexigénica– sometidos a una restricción de 20 kcal/kg/día, pero no así al hallarse en balance positivo. Subrayar que estos niveles aumentados de grelina durante la restricción de sueño reducen el gasto energético, estimula la sensación de hambre e ingesta de alimentos, promueve la retención de grasa y aumenta la producción de glucosa a nivel hepático para garantizar la disponibilidad de combustible a los tejidos dependientes de glucosa.
Sabemos que la pérdida de reservas energéticas por medio de cambios en la composición corporal se ve acompañada de compensaciones metabólicas, neuroendocrinas y conductuales a fin de contener la reducción en la tasa metabólica en reposo. Es decir, hablaríamos mecanismos de supervivencia sujetos a nuestra propia evolución. En este caso concreto, la tasa metabólica en reposo fue menor en el grupo de 5.5 horas vs 8.5, por lo que se produjo dicha adaptación metabólica. Por tanto, la compensación metabólica mejorada en forma de aumento del hambre y el gasto energético reducido observados en respuesta a la restricción combinada de calorías y sueño podría alterar la adherencia a una dieta de menor energía y promover además una recuperación del peso toda vez suspendida.
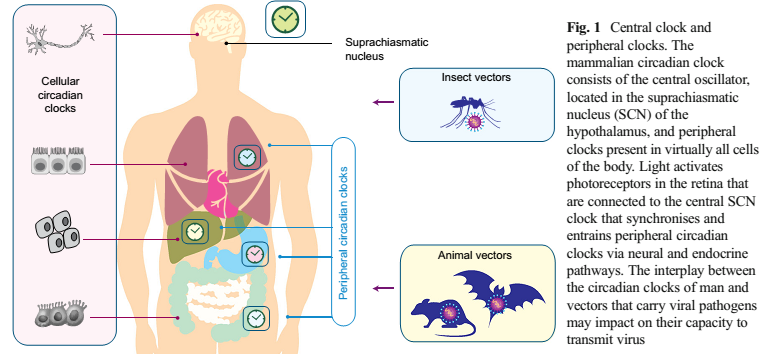
Al respecto de estas idas y venidas en el uso de los distintos sustratos energéticos y aumento o reducción de la tasa metabólica, trabajos en los que se lleva a cabo la eliminación del gen BMAL1, el cual se halla implicado en la regulación de los ritmos circadianos manteniendo un diálogo constante con el CLOCK, aquel otro que afecta a la persistencia y duración de estos ritmos, logran igualmente una alteración en la utilización de los sustratos energéticos en ratones, algo que también observamos en humanos por medio de la desincronización circadiana, disminuyendo además la tasa metabólica basal. Como curiosidad al respecto del gen BMAL1, decir que una disrupción en el mismo se ha observado en trabajos de laboratorio que aumenta la capacidad de replicación de los virus de la gripe y el herpes. Dicho de otro modo, las células arrítmicas desde el punto de vista circadiano serían más fácilmente asediadas por estos virus, de modo que estas disrupciones en BMAL1 favorecerían la replicación de los mismos, como ocurriría frente a la deprivación de sueño. Tan es así, que se ha observado cómo en personas mayores de 65 años, el momento de vacunación para la gripe –mañana o tarde– es un determinante en la respuesta a la inmunización sistémica.
Así las cosas, como resumen, podríamos subrayar el modo en que la disrupción recurrente del sueño y el ritmo circadiano facilitaría el desarrollo y mantenimiento de la obesidad mediante reprogramaciones en el ADN por medio de metilaciones y otras modificaciones epigenéticas en el tejido adiposo a favor de la adipogénesis y lipogénesis, así como una pérdida de masa muscular paralela. Es decir, la deprivación del sueño produciría una auténtica poda epigenética, un basto trabajo de jardinería que acabaría con los simétricos y floridos parterres de nuestro reloj interno para levantar en su lugar un abigarrado campo de hojarasca seca vía reprogramaciones epigenéticas capaces de gatillar según qué fenotipos clínicamente relevantes. La cronobiología aún tiene mucho que decir. Mientras tanto, incidamos en que el contar ovejitas sirve para algo más que pasar la mona.
REFERENCIAS:
-Cedernaes et al. Acute sleep loss results in tissue-specific alterations in genome-wide DNA methylation state and metabolic fuel utilization in humans Sci. Adv. 2018;4:eaar8590
-AV Nedeltcheva el al. Insufficient sleep undermines dietary efforts to reduce adiposityAnn Intern Med. 2010 October 5; 153(7): 435–441
-R Edgar et al. Cell autonomous regulation of herpes and influenza virus infection by the circadian clock. Proc Natl Acad Sci U S A. 2016 Sep 6;113(36):10085-90
-Cedernaes et al. Acute sleep loss results in tissue-specific alterations in genome-wide DNA methylation state and metabolic fuel utilization in humans Sci. Adv. 2018;4:eaar8590
-AV Nedeltcheva el al. Insufficient sleep undermines dietary efforts to reduce adiposityAnn Intern Med. 2010 October 5; 153(7): 435–441
-R Edgar et al. Cell autonomous regulation of herpes and influenza virus infection by the circadian clock. Proc Natl Acad Sci U S A. 2016 Sep 6;113(36):10085-90

 Fuente RSS
Fuente RSS

